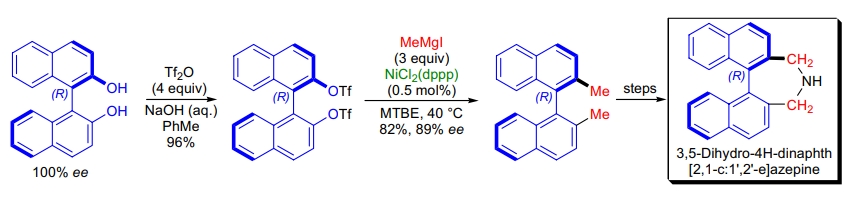
Kumada 交叉偶联反应
重要性
[开创性文献1-4;综述5-18;改进与优化19-30]
重要性
20 世纪 70 年代,大量研究集中于通过过渡金属催化,实现卤代烯基和芳基化合物的碳-碳键形成反应31,32。1972 年, M. Kumada 和 R.J.P. Corriu 分别独立报道了在镍-膦配合物催化下,芳基或烯基卤化物与 Grignard 试剂之间的立体选择性交叉偶联反应。 随后,Kumada 对该反应的适用范围和局限性进行了深入研究。如今,这一转化被称为 Kumada 交叉偶联反应。
反应特点
该反应的主要特点包括:
- 镍催化过程中,催化活性在很大程度上取决于膦配体的性质,其反应性顺序为:Ni(dppp)Cl2 > Ni(dppe)Cl2 > Ni(PR3)2Cl2 ~ Ni(dppb)Cl2;
- 即使含有 β-氢的烷基 (sp3) Grignard 试剂,也可以选择性地进行交叉偶联,而不会发生 β-氢消除;
- 对于仲烷基 Grignard 试剂,烷基基团往往会异构化为相应的正烷基基团,这种异构化依赖于膦配体的碱性和芳基卤化物的性质;
- 使用 dppf 配体可以显著减缓 β-氢消除并加速还原消除,从而允许仲 Grignard 试剂在没有异构化的情况下进行偶联24;
- 氯代芳烃可以轻松发生反应,甚至氟代苯也能发生镍催化的交叉偶联16;
- 反应具有立体选择性,起始烯基卤化物的立体化学结构可以保留;
- 钯催化过程具有更高的化学选择性和立体选择性,且与镍催化相比,其适用范围更广,但仅适用于芳基溴化物和碘化物,不能适用于芳基氯化物;
- 常用试剂包括有机镁和有机锂试剂,但偶联反应也可与有机钠 (RNa)、有机铜 (R2CuLi)、有机铝、有机锌、有机锡、有机锆和有机硼化合物进行14;
- 有机锂试剂是最具多样性的试剂,因为它们可以通过多种方法制备,包括直接锂化碳氢化合物9;
- 由于有机镁和有机锂化合物的极性特性,含有碱敏感官能团的底物不适合反应,这种耐受性在 Negishi 交叉偶联中通过使用低碱性的有机锌化合物得到了显著改善。
副反应及避免方法
尽管 Kumada 交叉偶联反应的副反应较少,但偶尔会出现偶联和还原产物的副产物。可通过以下措施避免这些副反应:
- 缓慢加入有机锂试剂,因为快速加入会生成 α-溴烯基锂,它们会发生重排生成锂乙炔,从而降低整体产率;
- 确保 Pd(0) 催化剂纯净以保持高活性;
- 避免试剂过量添加。
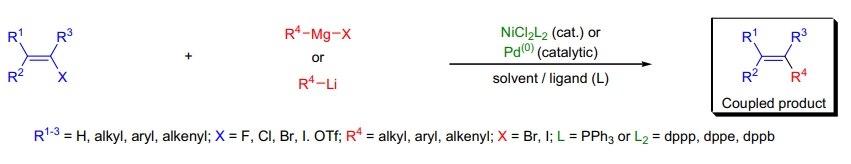
机理
[参考文献34-38]
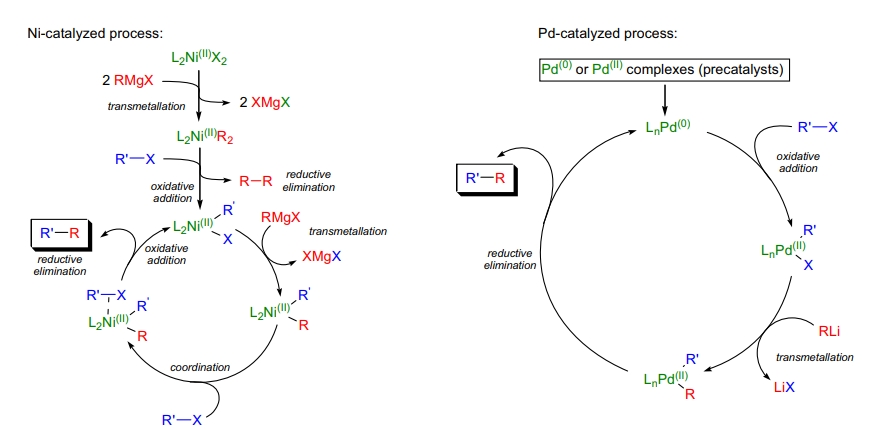
Kumada 交叉偶联反应的机理涉及氧化加成、转金属化和还原消除等关键步骤。在镍催化的情况下,氧化加成产生 Ni(II) 中间体,与 Grignard 试剂发生转金属化生成 Ni(II)-烷基中间体,最终经过还原消除生成目标交叉偶联产物。
合成应用
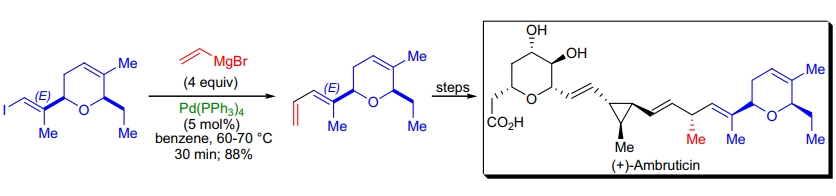
1. (+)-Ambruticin 的全合成: 在 E.N. Jacobsen 的研究中,Kumada 交叉偶联用于将 (E)-烯基碘转化为共轭二烯,保持了起始物的立体化学39。
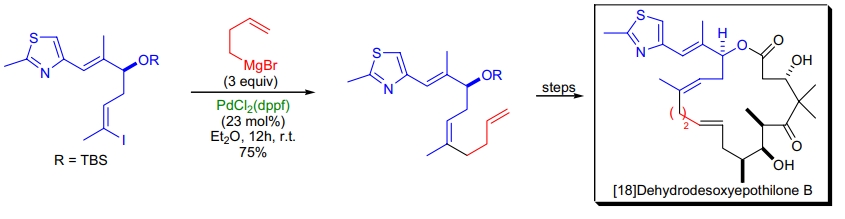
2. [18]Dehydrodesoxyepothilone B 的合成: S.J. Danishefsky 等通过 Kumada 交叉偶联将 (Z)-烯基碘前体转化为 1,5-二烯,以用于后续的环加成40。
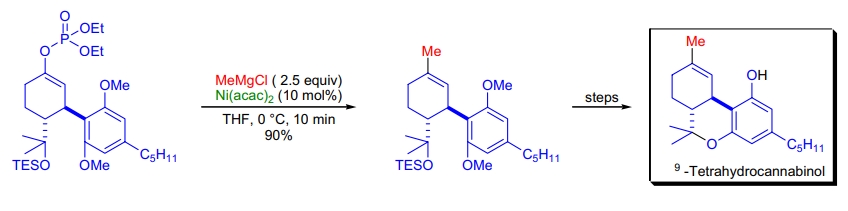
3. 四氢大麻酚类似物的合成: Y. Kobayashi 等人利用 Kumada 交叉偶联完成了酮类底物的功能化,得到目标二烯化合物41。
4. (R)-3,5-二氢-4H-双萘并[2,1-c:1',2'-e]氮杂环庚烷的合成: M. Ikunaka 等利用 Kumada 交叉偶联高效引入甲基,开发了短而可扩展的合成路线42。