Luche 还原反应
重要性
[开创性文献1-4;综述5-11;改进与优化12-15;理论研究16]
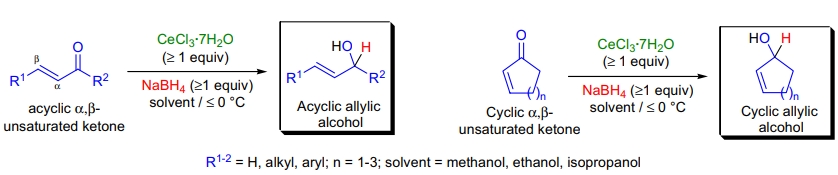
1978年,J.L. Luche 报道了使用镧系金属氯化物和硼氢化钠(NaBH4)选择性将α,β-不饱和酮还原为烯丙醇的方法。此反应,即 Luche 还原反应,解决了金属氢化物通常会导致 1,2- 和 1,4-加成混合产物的问题。
- 适用于直链和环状 α,β-不饱和酮,产物中几乎不含 1,4-还原副产物。
- CeCl3·7H2O 是反应中最有效的镧系盐。
- 大多数官能团(如羧酸、酯、酰胺、卤代烷、缩醛、硫化物、叠氮化物、环氧化物、硝基化合物)在反应条件下不受影响。
- 通常在室温或更低温度下进行,反应时间为 5-10 分钟。
- 反应对水和氧气不敏感,不需要惰性气氛,也无需对反应容器和溶剂进行干燥。
- 甲醇是最常用的溶剂,因其反应速率最高,但乙醇和异丙醇也偶尔被使用,尽管反应较慢。
- 立体阻碍对区域选择性影响甚微。
- CeCl3/NaBH4 对酮在醛存在下的化学选择性非常高,因为醛在这些条件下会迅速发生缩醛化,避免被还原。
- 环己烯酮的取代物主要发生氢化从轴向进攻,生成赤道位的醇。
- 在刚性环状或多环体系中,氢化通常从羰基的最少位阻面发生。
- 共轭或芳香醛优先于孤立的脂肪醛被还原。
- 将反应温度降至 -78°C 以下,能显著提高手性底物还原的非对映选择性。
机理
[参考文献17,4,18]
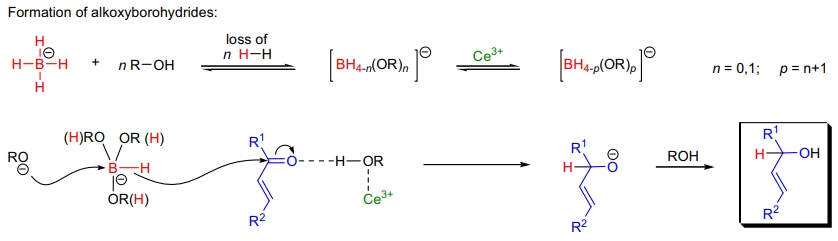
Luche 还原反应的活性物种是醇氧基硼氢化物,结合了硬性 Ce3+,使其作为硬性还原剂选择性作用于羰基。Ce3+ 还通过协调醇氧基增加溶剂酸性并间接活化羰基。
合成应用
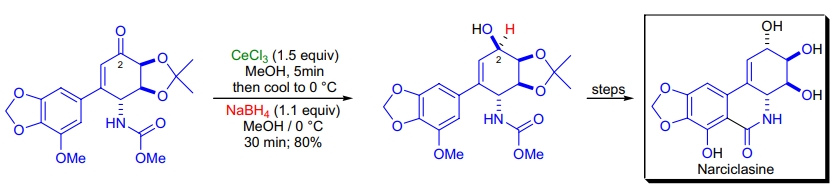
1. Narciclasine 的全合成: T. Hudlicky 等人通过 Luche 还原建立了 C2 立体化学。α,β-不饱和环酮在 CeCl3/NaBH4 存在下,羰基的氢化从空间位阻较小的一面进行21。
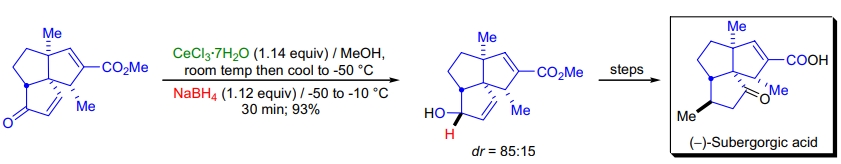
2. Subergorgic Acid 的全合成: L.A. Paquette 使用 Luche 还原以 -50 °C 的低温反应获得高二面选择性产物22。
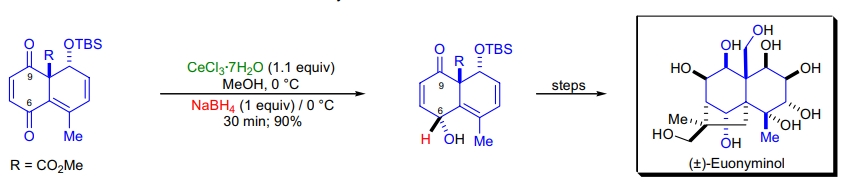
3. Euonyminol 的全合成: J.D. White 等人利用 Diels-Alder 反应构建关键中间体,随后进行 Luche 还原以实现区域和立体选择性还原23。