Malonic 酯合成反应
重要性
[开创性文献1,2;综述3-6;改进与优化7-16]
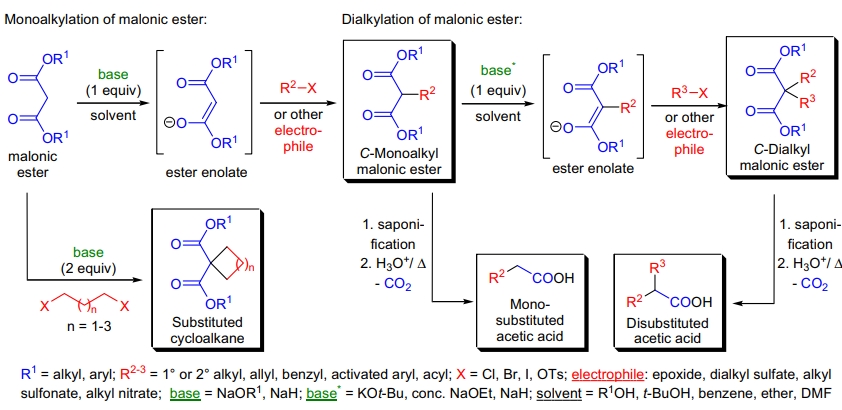
1863年,Geuther 首次通过活性亚甲基化合物的酯负离子与有机卤化物的反应实现了 C-烷基化反应,即 Malonic 酯合成反应。这一方法为取代乙酸衍生物的合成提供了有效途径。
- 丙二酸酯通常由脂肪族醇(如甲醇、乙醇、叔丁醇)衍生而来。
- 亚甲基的 pKa 通常在 9-11 之间,因此弱碱足以生成活泼的酯负离子。
- 碱的选择通常与酯基一致,以避免生成混合酯(如二甲基丙二酸酯用 NaOMe 和甲醇去质子化)。
- 反应溶剂可以是醇类(如甲醇、乙醇)、极性非质子溶剂(如 DMF)或非极性非质子溶剂(如苯)。
- 对于一级和二级烷基卤化物,反应通常通过双分子亲核取代(SN2)机制进行,高浓度的负离子和卤化物加速反应。
- 烯丙基和苄基卤化物可通过单分子亲核取代(SN1)机制反应。
- 一级、二级卤化物以及烯丙基和苄基卤化物反应最快,而三级卤化物主要生成消除产物。
- 卤化物的反应性顺序为 I ~ OTs > Br > Cl。
- C-单烷基化丙二酸酯的酸性低于未取代的丙二酸酯,因此需要更强的碱来实现二次去质子化,而对应的负离子烷基化速度较慢。
- 当使用 α,ω-二卤代物作为烷基化试剂时,可生成环烷烃,五元、六元和七元环的生成最为有利。
- 单取代或双取代丙二酸酯经碱性皂化生成 1,3-二酸,后者在酸性加热条件下脱羧生成取代乙酸。
机理
[参考文献18,4]
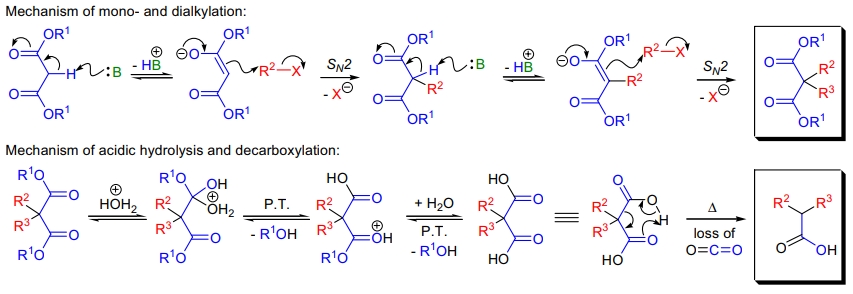
Malonic 酯合成反应的机理包括酯负离子的生成、与卤代烷的亲核取代反应、以及最终的皂化和脱羧过程。其机理过程高度依赖于底物的酸性和碱的选择。
合成应用
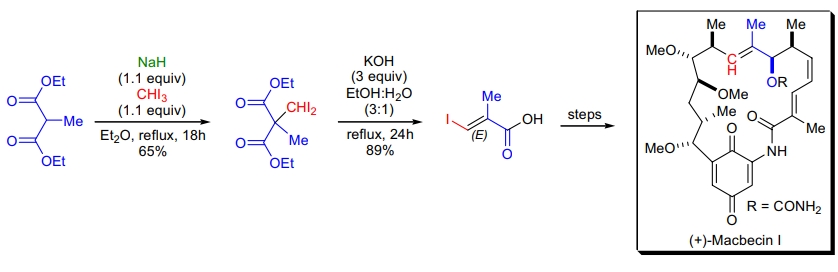
1. (+)-Macbecin I 的全合成: R. Baker 利用 Malonic 酯合成法制备关键的乙烯基碘化物中间体。在反应过程中,二乙基甲基丙二酸酯与二碘卡宾反应后,通过皂化和脱羧生成所需化合物19。
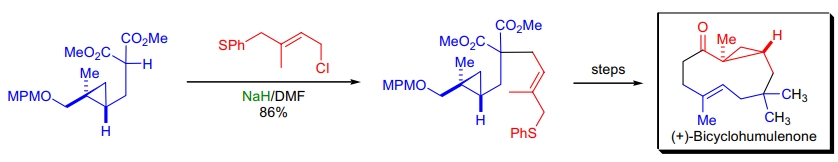
2. (+)-Bicyclohumulenone 的全合成: M. Kodama 使用 Malonic 酯合成将两片段结合,实现了 10 元环和环丙烷的立体选择性构建20。
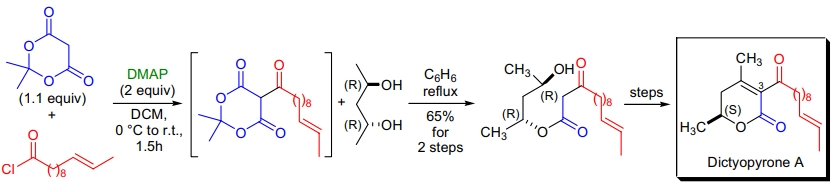
3. Dictyopyrone A 的全合成: Y. Oshima 利用 Malonic 酯合成法首次合成了具有 α-吡喃酮基团的天然产物 Dictyopyrone A21。