Mannich 反应
重要性
[开创性文献1-3;综述4-23;改进与优化24-36]
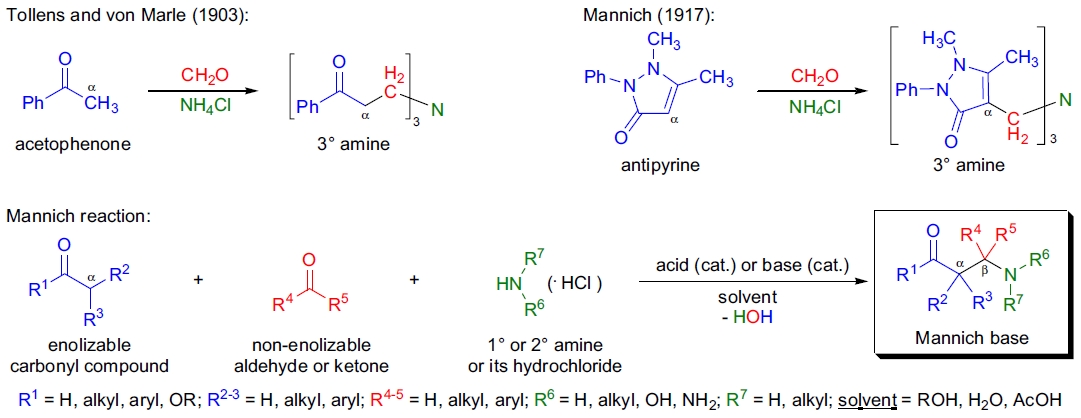
Mannich 反应是通过 CH 活性化合物(如醛或酮)与一元或二元胺(或氨)以及非烯醇化醛(或酮)的缩合反应生成氨基烷基化衍生物的反应。这种反应生成的 β-氨基羰基化合物被称为 Mannich 碱,是一种重要的合成中间体。
- CH-活化化合物通常为脂肪族或芳香族醛酮、羧酸衍生物、β-二羰基化合物、硝基烷或富电子芳香化合物(如酚,发生邻位反应)以及末端炔烃12,13。
- 仅一级和二级脂肪胺或其盐酸盐可用,芳香胺通常不参与反应。
- 最常见的非烯醇化羰基化合物为甲醛。
- 当胺组分为一级胺时,最初生成的 β-氨基羰基化合物可进一步反应生成 N,N-二烷基衍生物(三级胺);二级胺不会发生过度烷基化。
- 通常使用的反应介质为乙醇、甲醇、水或醋酸等质子溶剂,以确保足够浓度的电亲核亚胺离子。
- 不对称酮通常生成区域异构的 Mannich 碱,但更取代的 α-位产物通常为主要产物。
- Mannich 碱是有价值的合成中间体,可通过以下转化生成多样化的化合物:
- β-消除生成 α,β-不饱和羰基化合物(Michael 受体);
- 与有机锂试剂或 Grignard 试剂反应生成 β-氨基醇;
- 用亲核试剂取代二烷基氨基基生成功能化羰基化合物。
机理
[参考文献6,50,12-14]
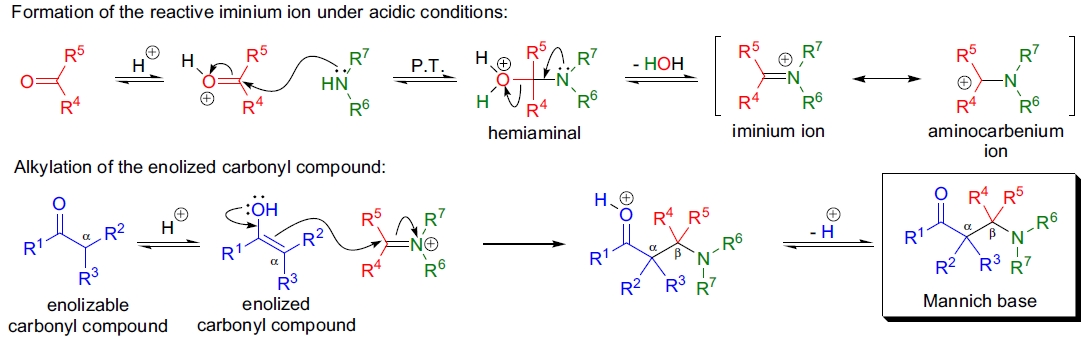
Mannich 反应通常在酸性条件下进行。首先,胺与质子化的非烯醇化羰基化合物反应生成亚胺盐,该亚胺盐与羰基化合物的烯醇形式发生加成反应,生成 β-氨基羰基化合物。
合成应用
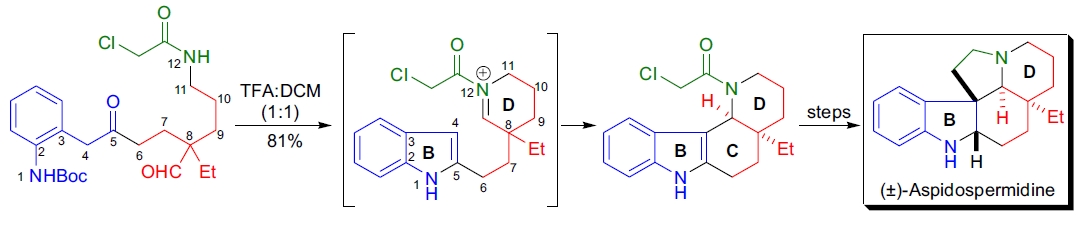
1. (±)-Aspidospermidine 的全合成: C.H. Heathcock 等人在全合成中使用 Mannich 反应完成了 B、C 和 D 环的构建。底物在三氟乙酸的作用下,通过 Mannich 型环化反应形成所需结构51。
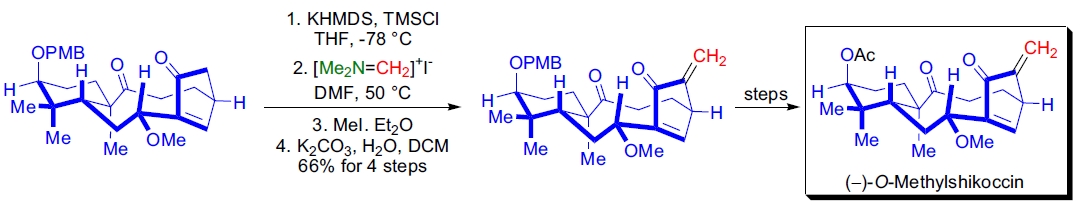
2. (–)-O-Methylshikoccin 的全合成: L.A. Paquette 利用 Eschenmoser 盐与金属烯醇盐的 Mannich 反应,在区域选择性上实现了高效的外亚甲基功能化52。
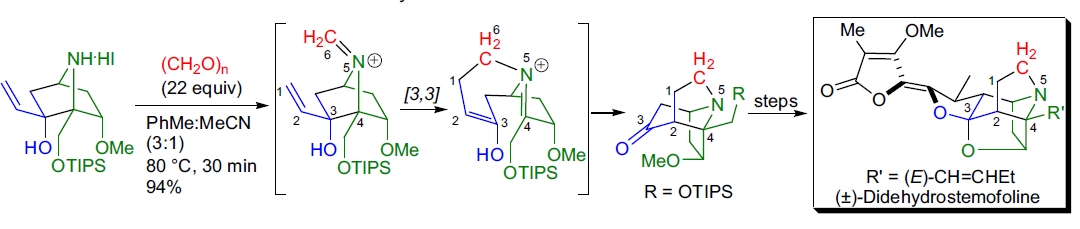
3. (±)-Didehydrostemofoline 的全合成: L.E. Overman 等人将 Mannich 反应与 aza-Cope 重排反应结合,完成了复杂杂环的高效构建53。