Michael加成
重要性
[开创性文献1-4;综述5-26;改进与优化27-46;理论研究47-66]
背景与历史
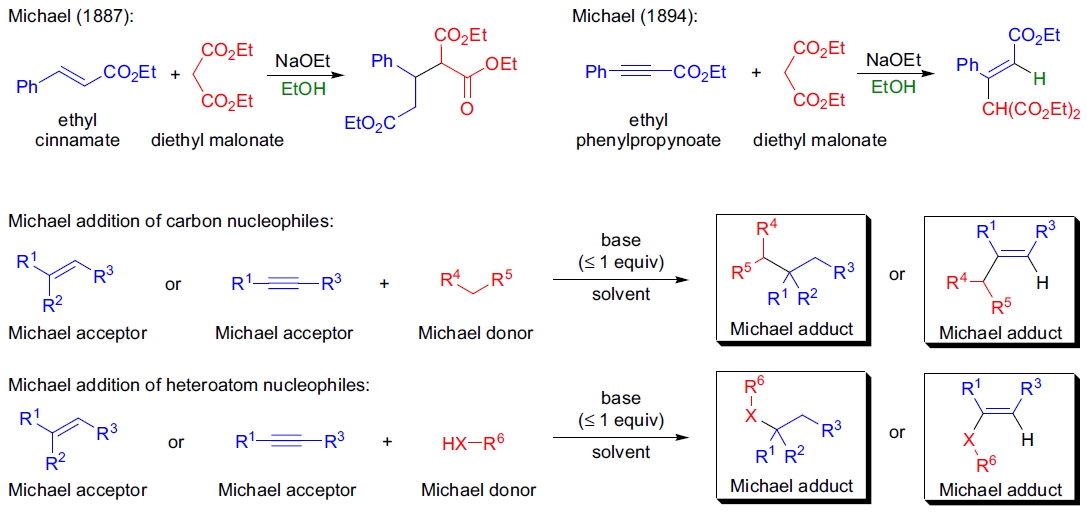
1883年,T. Komnenos 观察到二乙基丙二酸的阴离子可与亚乙基丙二酸反应生成产物,这是首例碳亲核试剂加成至电子缺乏双键的例子1。 到1887年,A. Michael 系统研究了稳定阴离子的 α,β-不饱和体系加成,发现二乙基丙二酸在乙醇钠存在下可与肉桂酸乙酯反应生成取代的戊二酸二酯2。 他还证明了电子缺乏的三键同样可作为碳亲核试剂的反应底物4。
反应概述
Michael 加成是指稳定碳亲核试剂对活化的 π-体系(如α,β-不饱和酯、酮)的 1,4-加成。其主要特点包括:
- 亲核试剂(Michael 供体)通常由活性甲烷化合物(如醛、酮、腈、β-二羰基化合物等)脱质子化生成。
- 根据电子吸引基团的类型和强度,即使使用弱碱(如三乙胺)也能实现反应。
- 反应可使用催化量的碱,当使用一当量碱时,产物阴离子可与其他亲电试剂进一步反应。
- 活化烯烃或炔烃(Michael 受体)的结构多样化,几乎任何电子吸引基团均可使用。
- 反应可在亲质子或非亲质子溶剂中进行。
- 存在多种分子内和分子间版本。
- 当 Michael 供体和受体具有明确的立体化学时,反应可高度非对映选择性。
- 发展出了多种不对称版本的 Michael 加成。
机理
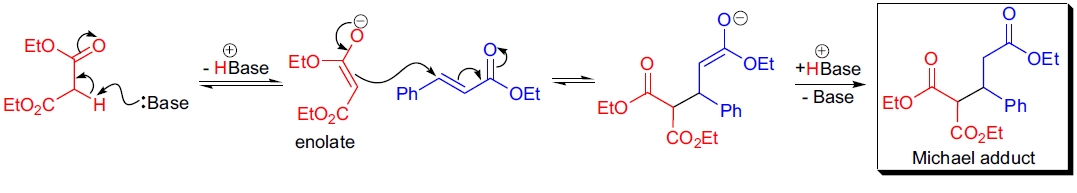
[参考文献9,11,67,17]
以丙二酸二乙酯阴离子与肉桂酸乙酯的加成为例,Michael 加成通过亲核试剂对双键的 1,4-加成实现。 在亲质子溶剂中,反应可逆,产物通常为热力学上最稳定的异构体。当使用金属有机试剂(如铜催化的格氏试剂)时,可能涉及单电子转移(SET)机理。
合成应用
-
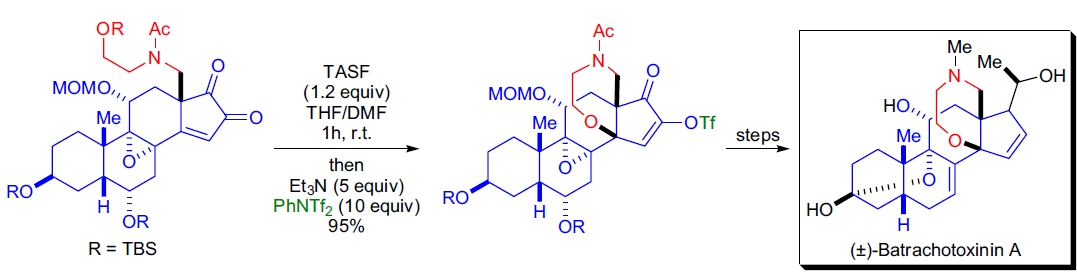
**(±)-Batrachotoxinin A 的全合成**: 关键步骤通过 Michael 加成形成七元氧氮杂环。
-
**Fredericamycin A 的全合成**: 通过串联 Michael 加成-Dieckmann 缩合构建复杂的三环体系。
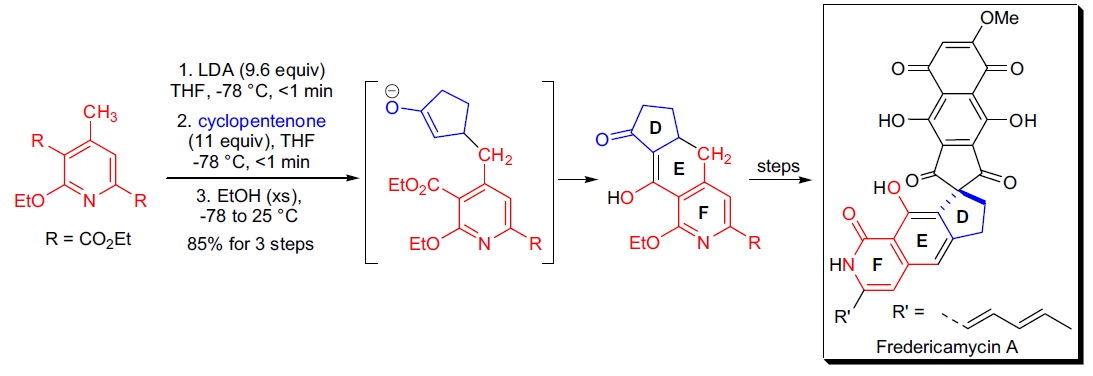
-
**(±)-Longiborneol 的合成**: 通过分子内双 Michael 加成高效构建三环体系。
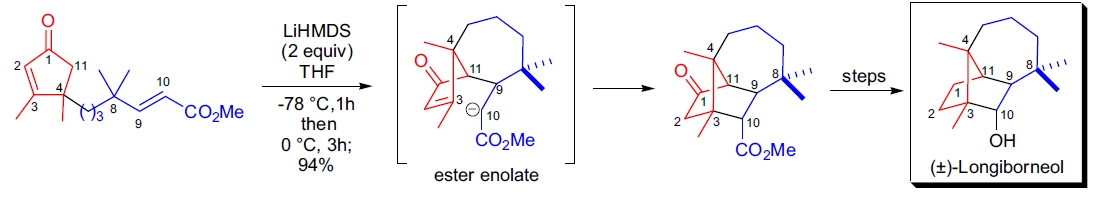
-
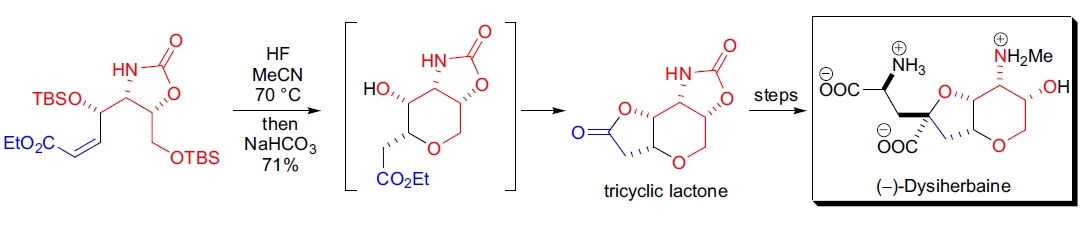
**(–)-Dysiherbaine 的全合成**: 通过分子内 Michael 加成构建中心吡喃环。