Mitsunobu 反应
重要性
[开创性文献1-3;综述4-12;改进与优化13-24]
背景与历史
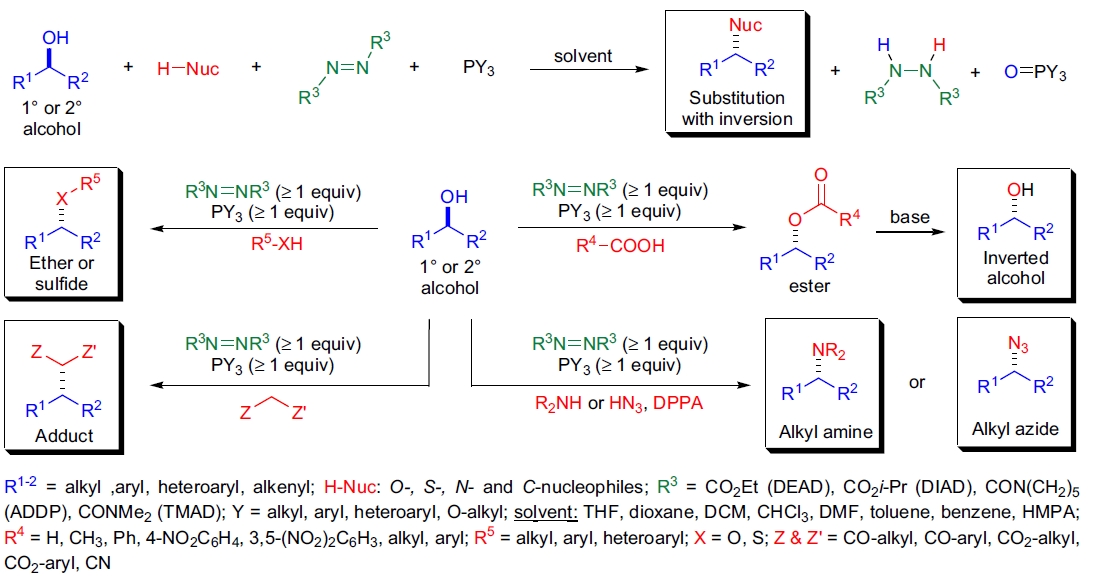
1967年,O. Mitsunobu 等人报道了仲醇在二乙基偶氮二甲酸酯(DEAD)和三苯基膦存在下高效酰化的现象1,2。 随后发现光学活性仲醇在该反应条件下发生完全构型翻转。此后,该方法被广泛应用于手性胺、叠氮化物、醚、硫醚,甚至烷烃的合成。 在二烷基偶氮二甲酸酯和三烷基或三芳基膦存在下,醇与亲核试剂的取代反应被称为 Mitsunobu 反应。
反应概述
Mitsunobu 反应的主要特点如下:
- 一醇和仲醇是最好的底物,仲醇经历完全构型翻转。
- 叔醇一般不参与反应,但某些叔丙炔醇可成功转化。
- 亲核试剂通常是相对酸性的化合物(pKa ≤ 15)。
- 氧亲核试剂中,羧酸生成酯,醇和酚生成醚,而硫醇和硫酚生成硫醚。
- 常见的氮亲核试剂包括酰亚胺、羟肟酸酯、含氮杂环和叠氮化氢。
- 可形成碳-碳键,但亲核试剂通常为活性亚甲基化合物(如β-二酮和β-酮酯)。
- 该反应还可进行分子内转化,制备3-7元环的醚和胺。
- 在卤化物源存在下(如卤化烷和卤化锌),醇可转化为对应的卤化物。
- 反应一般在THF中进行,也可使用二噁烷和二氯甲烷。
- 最常用的膦试剂是 PPh3 或 P(n-Bu)3。
- 二乙基偶氮二甲酸酯(DEAD)和异丙基偶氮二甲酸酯(DIAD)可互换使用。
- 反应温度通常在 0 °C 至 25 °C 之间,但某些空间位阻大的底物可能需要更高温度。
机理
[参考文献25-45]
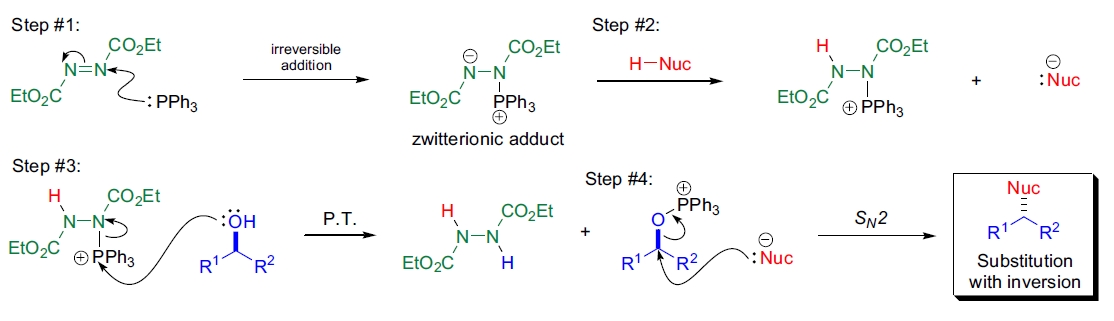
Mitsunobu 反应的机理包括醇与三苯基膦和二乙基偶氮二甲酸酯反应形成磷鎓盐中间体,随后亲核试剂取代醇中的羟基, 同时发生构型翻转。该过程通过协同机制完成,生成的副产物(如膦氧化物)易于分离。
合成应用
-
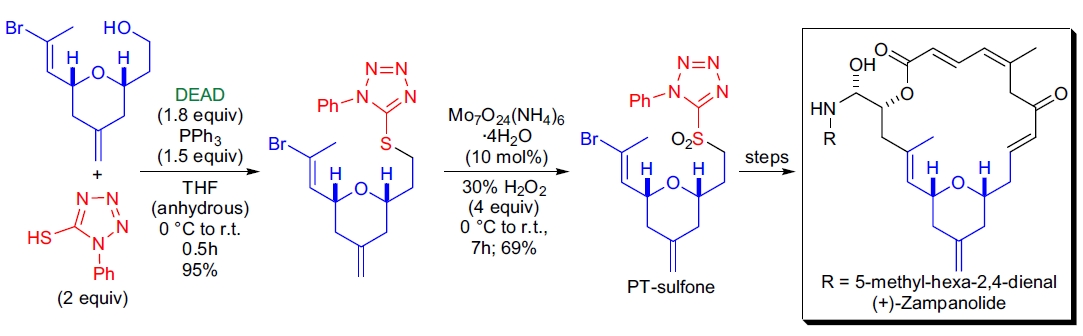
**(+)-Zampanolide 的全合成**: A.B. Smith 团队在合成该巨环内酯时,利用 Mitsunobu 反应构建了关键的 PT-砜基中间体。
-
**ent-WIN 64821 的合成**: L.E. Overman 实验室利用 Mitsunobu 反应完成了两个 C-N 键的立体专一性引入。
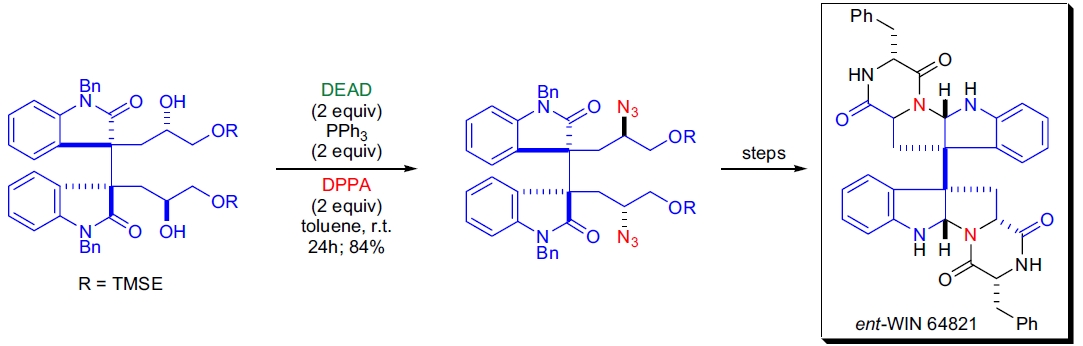
-
**(+)-Duocarmycin A 的合成**: D.L. Boger 等人利用 Mitsunobu 条件实现了新碳-碳键的跨环螺环化。
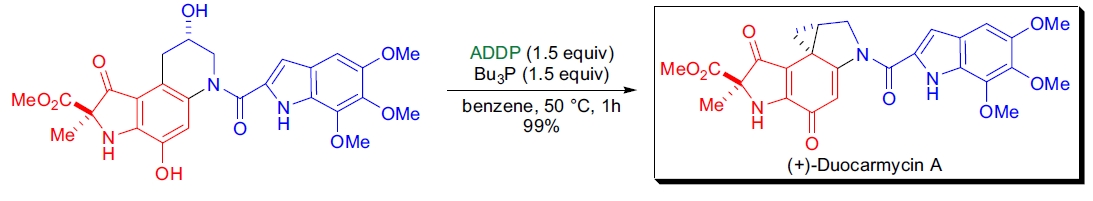
-
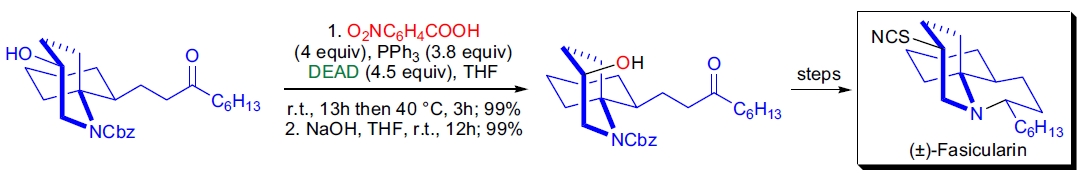
**(±)-Fasicularin 的全合成**: C. Kibayashi 团队通过 Mitsunobu 反应翻转仲醇的构型,最终完成天然产物的合成。