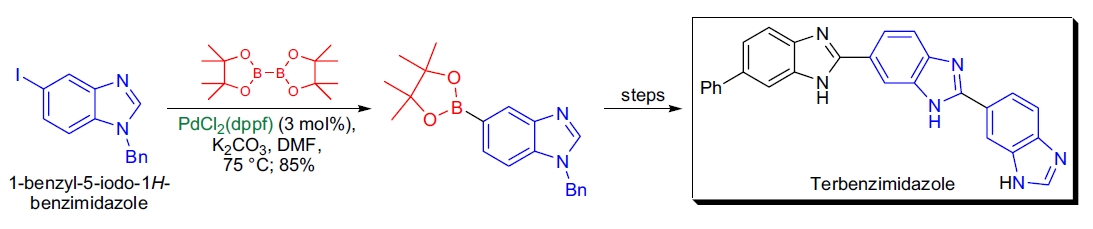
Miyaura 硼化反应
重要性
[开创性文献1-2;综述3-12;改进与优化13-31]
背景与历史
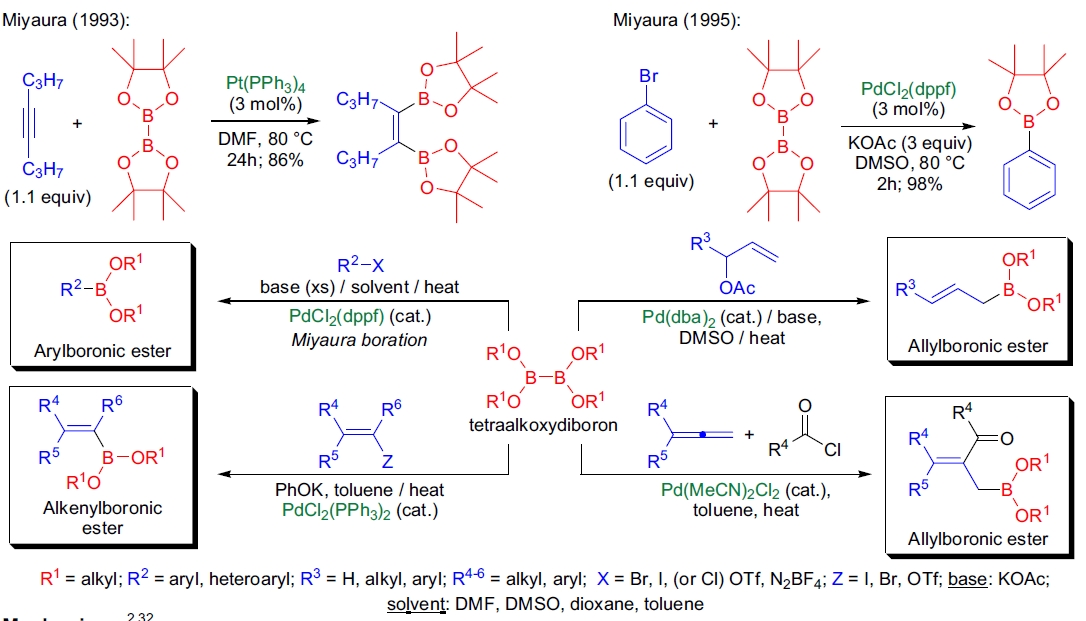
1993年,N. Miyaura 等人发现,炔烃在铂催化剂四三苯基膦配合物存在下,与二硼酸的邻二苯二醇酯(B2pin2 或 pinB-Bpin)发生高效的顺式双硼化反应1。 1995年,他们进一步发现四烷氧基二硼化合物可与芳基卤代物在 PdCl2(dppf) 催化剂存在下耦合,生成芳基硼酸酯。这种反应是 Suzuki 偶联和 Ullmann 联芳醚合成的重要底物来源2。 令人惊讶的是,仅钯基催化剂能有效催化此反应,其他金属配合物则完全无效。
反应概述
Miyaura 硼化反应的主要特点如下:
- 单锅反应条件温和,显著优于传统芳基硼酸酯和硼酸合成方法(如三烷基硼酸酯与芳基卤代物或芳基锂反应)。
- 在温和的碱性条件下,大多数官能团可以耐受。
- 最佳底物为芳基溴化物和碘化物,近年来也报道了芳基三氟甲磺酸酯和芳基重氮四氟硼酸盐的应用15,3,21。
- 芳基可带有电子供体或电子受体取代基。
- 电子富集的芳基溴化物反应速度较慢,而电子富集的芳基碘化物则反应较快,因此可以高产率实现芳基碘化物在芳基溴化物存在下的化学选择性硼化。
- 使用 Pd(0)-三环己基膦作为催化剂,可以使反应适用于活性较低的芳基氯化物23。
- 反应混合物中加入乙酸钾(KOAc)作为碱对于芳基卤代物的成功耦合至关重要,不仅能加速反应,还能防止联芳副产物的形成(Suzuki 偶联)。
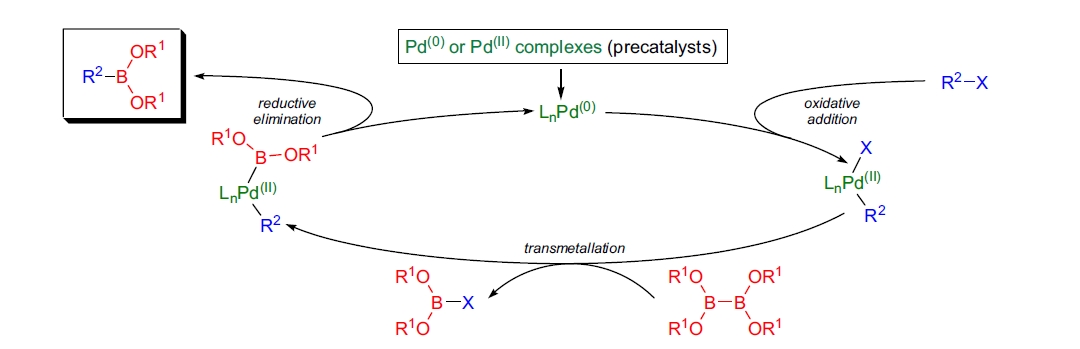
机理
[参考文献2,32]
Miyaura 硼化反应的第一步是钯(0)配合物对芳基卤代物 C-X 键的氧化加成。随后发生易位金属化,具体机制取决于底物的性质,最终还原消除生成目标产物。
合成应用
-
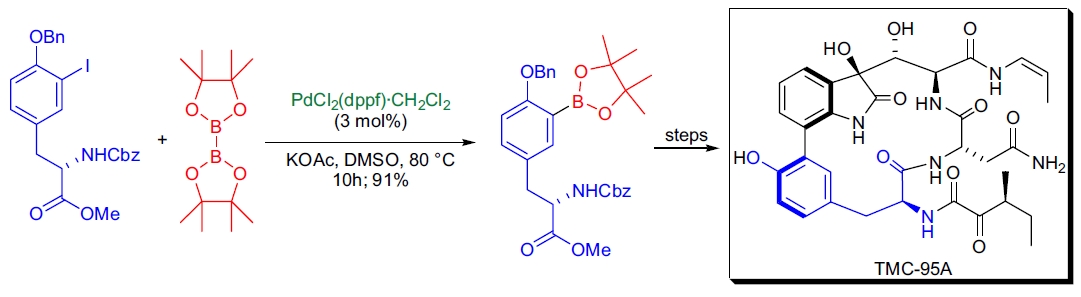
**TMC-95A 的全合成**: S.J. Danishefsky 团队利用 Miyaura 硼化反应制备了关键的芳基硼酸酯中间体。
-
**含联芳基的大环化合物的合成**: J. Zhu 实验室开发了基于 Miyaura 硼化和分子内 Suzuki 偶联的串联反应。
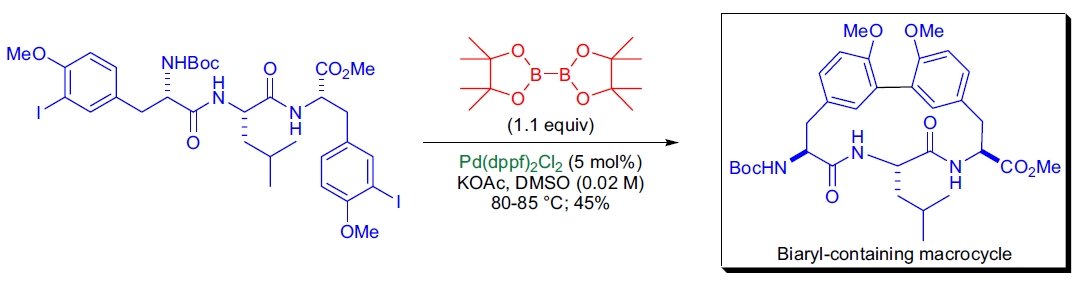
-
**(+)-Spiroxin C 的全合成**: T. Imanishi 等人利用 TBAF 激活的 Suzuki 偶联合成了目标天然产物。
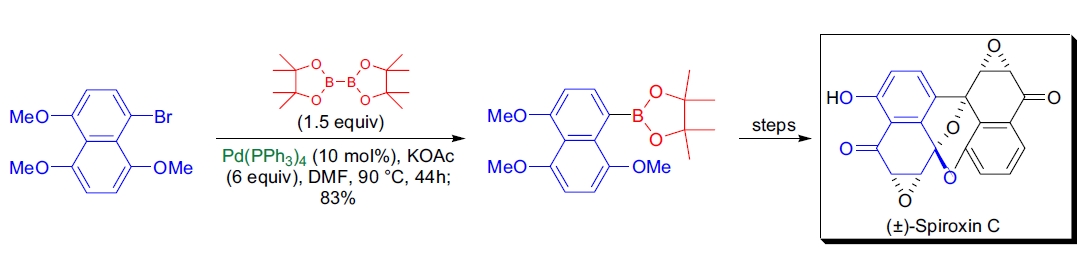
-
**Terbenzimidazole 的高效合成**: P.J. Smith 实验室通过 Miyaura 硼化反应制备了所需的芳基硼酸酯中间体。