Mukaiyama Aldol反应
重要性
[开创性文献1-2;综述3-16;改进与优化6,10-14,16]
背景与历史
1970年代初,T. Mukaiyama 报道了通过Lewis酸介导的硅烯醇与羰基化合物的加成反应实现交叉Aldol反应1,2。 这一反应大幅扩展了羰基化学的应用范围,成为有机合成中重要的碳-碳键形成反应之一。
反应概述
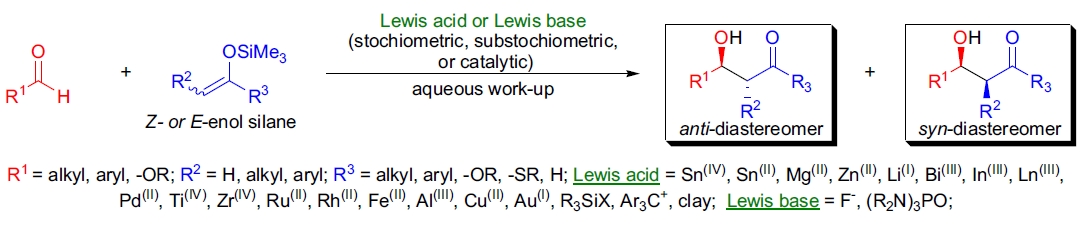
Mukaiyama Aldol反应的主要特点如下:
- Lewis酸(如TiCl4, SnCl4, ZnCl2)的化学计量用量曾是必要条件1,2,但近年来已开发出多种Lewis酸催化体系。
- 催化剂范围包括Sn(IV), Mg(II), Bi(III), Ti(IV), Cu(II), Au(I)等6,10,11,13,14。
- 硅烯醇可以从醛、酮、酯等制备,反应底物范围广泛4。
- 反应对diastereoselectivity具有显著调控潜力:
- 当R2较小且R3较大时,倾向于形成anti产物。
- 当R2较大时,syn选择性占优。
- 具有螯合能力的醛底物则优先生成syn构型产物。
- 通过使用手性硅烯醇或手性羰基化合物,可以实现对立体选择性的精准控制14。
Asymmetric catalytic processes是目前该领域发展的最前沿之一,已有多种手性Lewis酸和Lewis碱催化体系被开发13。
机理
[参考文献1-2,6,10,14]
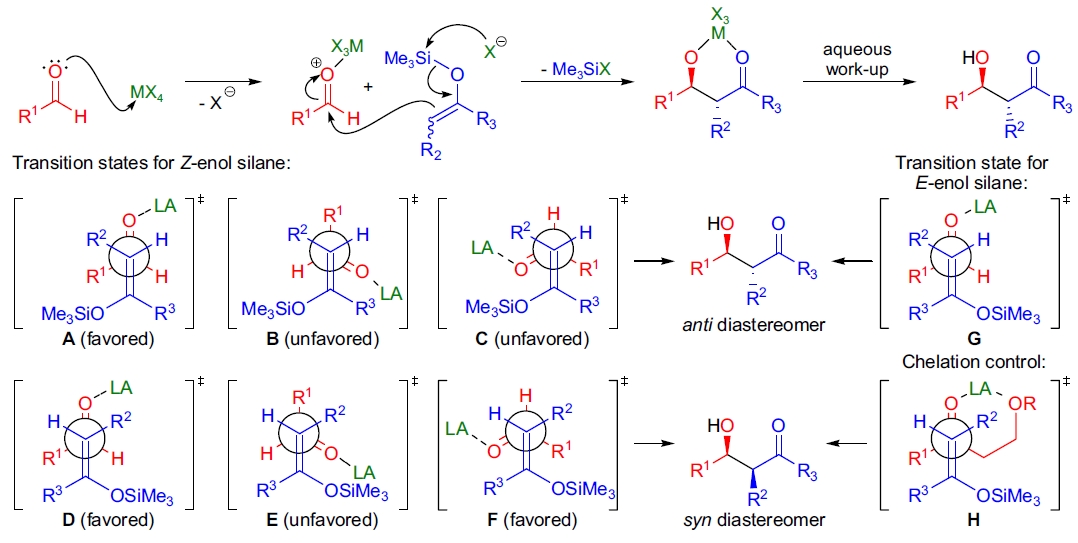
Mukaiyama Aldol反应的机理在很大程度上取决于反应条件、底物和Lewis酸的选择。在经典条件下(使用等摩尔的TiCl4),研究表明Lewis酸通过与醛组分配位进行活化30,31,35,随后迅速形成碳-碳键。硅基的转移可能以分子内或分子间的方式发生。 反应的立体化学结果通常通过开放过渡态模型进行解释,该模型基于立体效应和偶极效应14。对于Z-硅烯醇,过渡态A、D和F的能量接近。当取代基R2较小而R3较大时,过渡态A最为有利,生成anti-二面体异构体34。相反,当R2较大而R3较小时,过渡态D更占优势,生成syn-二面体异构体作为主要产物。当醛底物具有螯合能力时,反应可能通过过渡态H优先生成syn产物29,32,36。
合成应用
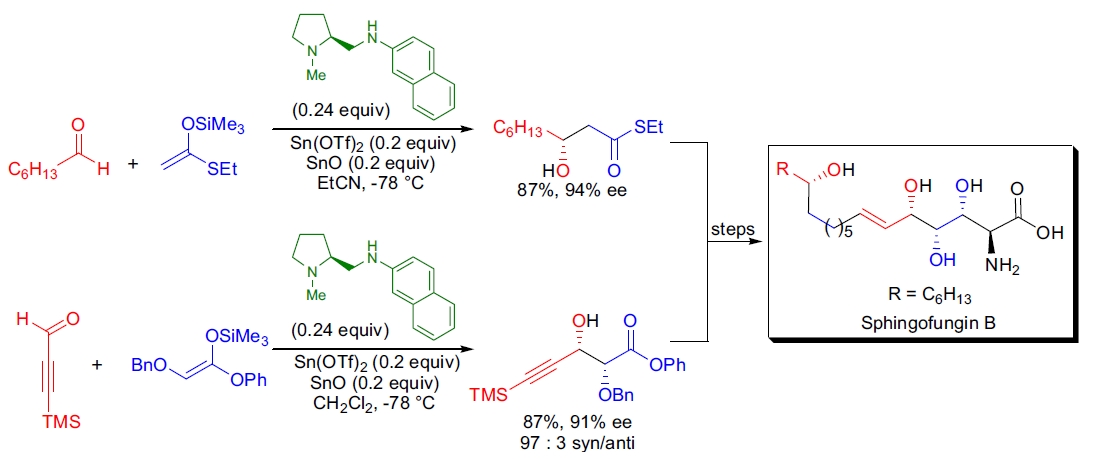
1. 多取代醇的合成: 使用Mukaiyama Aldol反应对手性醇进行立体专一性扩展15。
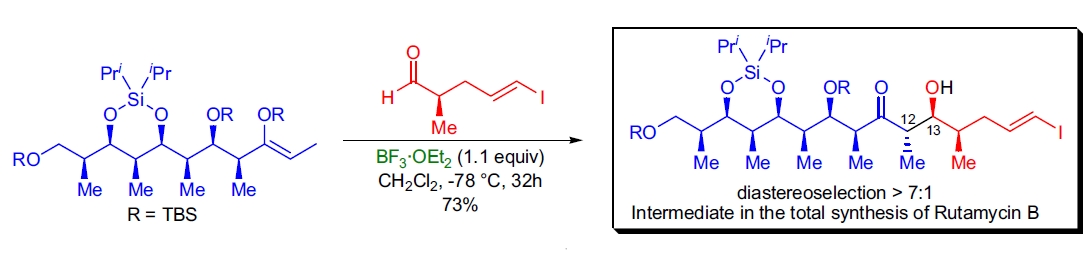
2. 天然产物的全合成: 多个研究中采用Mukaiyama Aldol反应构建复杂分子骨架16。