Staudinger reaction
重要性
[开创性文献1;综述2-15;改进与优化16-32;理论研究33-35]
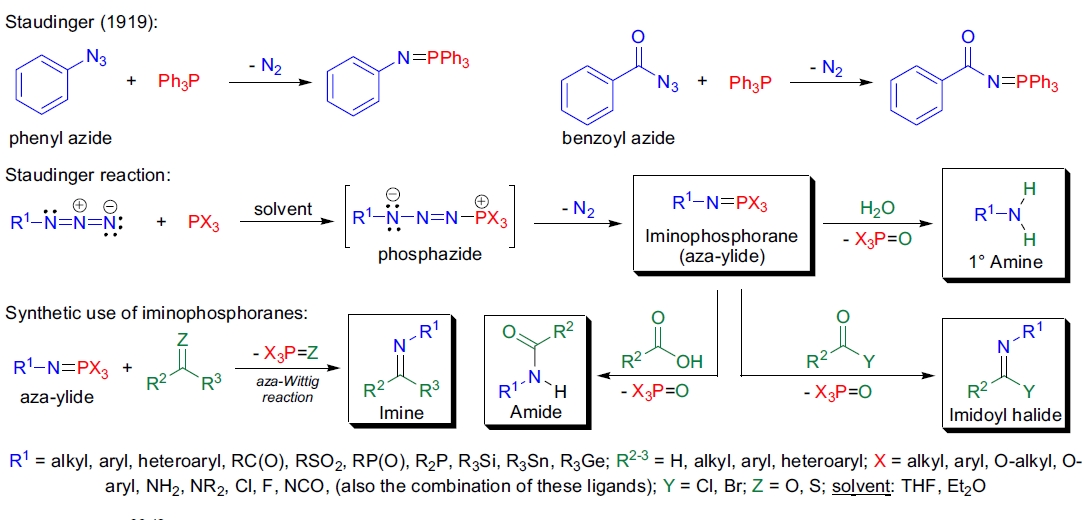
1919年,H. Staudinger和J. Meyer报道了苯基叠氮化物与三苯基膦的反应,生成一种新颖化合物膦亚胺(也称为aza-叶立德或亚胺膦),定量生成并伴随氮气逸出1。
他们发现苯甲酰叠氮化物以类似方式与三苯基膦反应,生成相应的苯甲酰膦亚胺,并研究了膦亚胺的反应性。
研究表明,膦亚胺与二氧化碳反应生成苯基异氰酸酯和三苯基膦氧,这是aza-Wittig反应的第一个例子。
有机叠氮化物与三价磷化合物(如三烷基或三芳基膦)反应生成相应膦亚胺的反应称为Staudinger反应。
该反应的主要特点包括:4,6,9,10
- 反应通常非常快,几乎定量生成产物且无副产物。
- 几乎任何三价磷化合物都可参与反应。
- 叠氮化物组分的结构可以有很大变化。
- 由烷基或芳基叠氮化物和三烷基或三芳基膦生成的膦亚胺产物是稳定的化合物,但膦原子上的烷氧基易发生烷基迁移。
膦亚胺是多功能的合成中间体,可通过以下方法进行转化:
- 与水水解生成伯胺(叠氮化物的这种还原高度化学和立体选择性)。
- 与羰基或硫羰基化合物进行分子内或分子间反应生成亚胺(aza-Wittig反应)。
- 与羧酸反应生成N-取代酰胺。
- 与酰卤反应生成亚胺基卤化物。
- 通过臭氧化生成硝基化合物。
机理36-42
Staudinger反应的机理已经被许多动力学和理论研究探讨,但目前具体机理尚不完全明确35。
所有实验数据表明,自由基或亚氮化合物不是反应中间体。
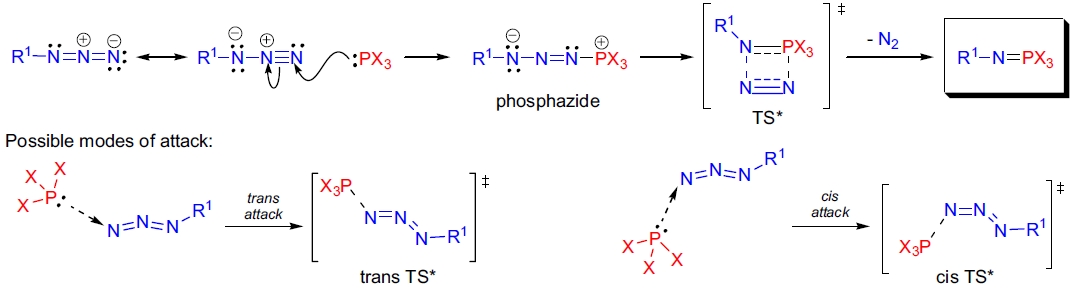
机理的第一步是叠氮化物的未取代氮原子(Nα)进攻三价磷,生成相应的膦叠氮化物(有时可以分离)且磷原子保持构型。
随后,膦叠氮化物通过一个四元过渡态失去氮气,生成膦亚胺。
关于磷原子如何进攻叠氮化物的Nα存在争议,因为P–N=N=N骨架并非线性,而是近似170°。
合成应用
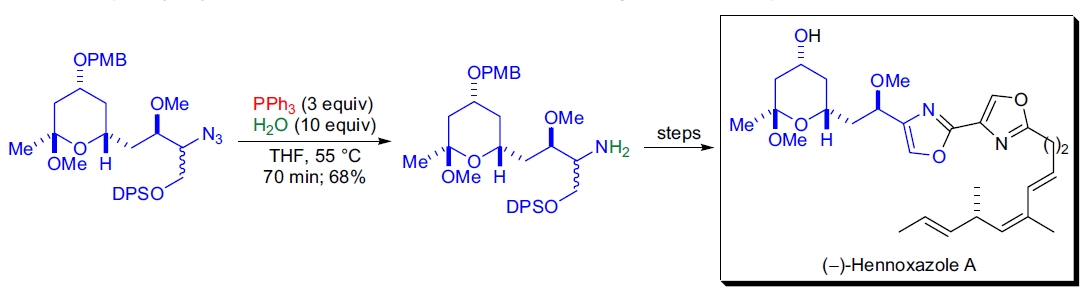
F. Yokokawa等人完成了抗病毒海洋天然产物(–)-hennoxazole A的全合成43。
在稍高温的THF/水混合溶液中,使用三苯基膦对C9的仲叠氮化物进行温和还原,得到对应的伯胺并随后酰化,形成天然产物的噁唑环之一。
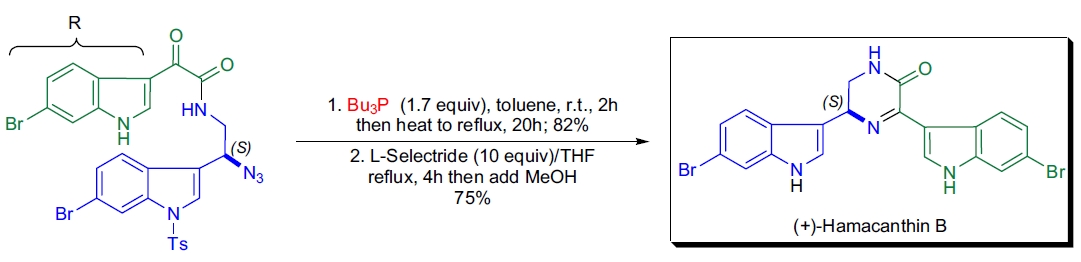
B. Jiang等人通过串联Staudinger反应/分子内aza-Wittig反应合成了(+)-hamacanthin B44。
该方法将仲叠氮化物转化为相应的膦亚胺,并通过加热使其环化生成中心吡嗪酮环。
叠氮化物的还原使用少量过量的三丁基膦在无水甲苯中进行,aza-Wittig环化需要回流温度。
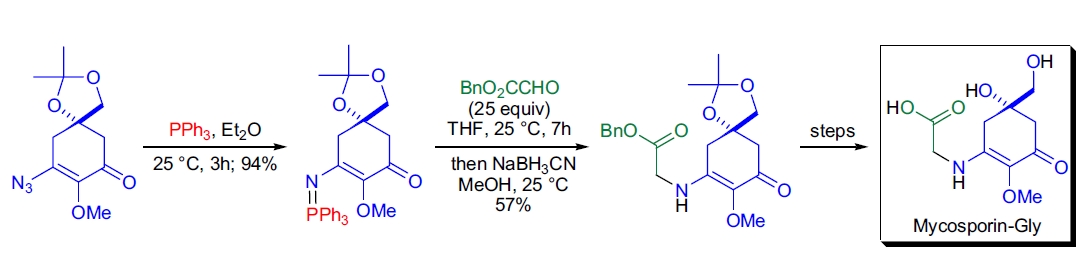
J.D. White实验室通过对真菌代谢物mycosporins的对映选择性全合成确定了其独特结构45。
在合成的最后阶段,利用Staudinger反应修饰侧链,将环状乙烯叠氮化物转化为稳定的乙烯膦亚胺,然后与苯甲醛乙酸反应生成对应的席夫碱。
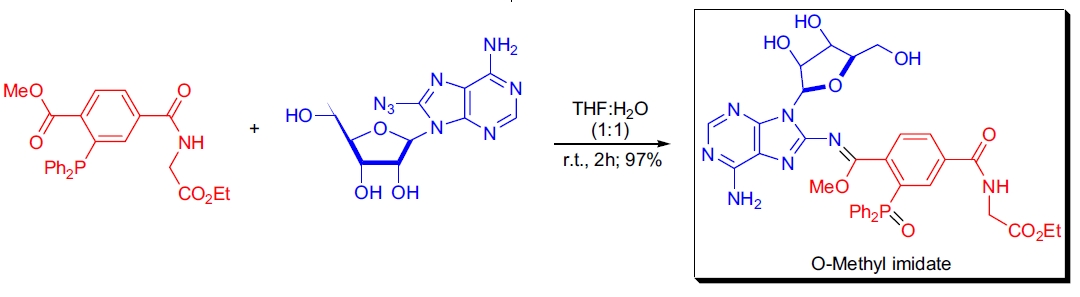
S.R. Rajski团队研究了o-羧烷基三芳基膦与芳基叠氮化物的反应,生成含O-烷基亚胺酸酯键的Staudinger连接产物27。
相比之下,烷基叠氮化物与o-羧烷基三芳基膦的反应通常生成酰胺键。该技术的价值在于其能够在生物相容条件下耦合非生物试剂。