转移氢化
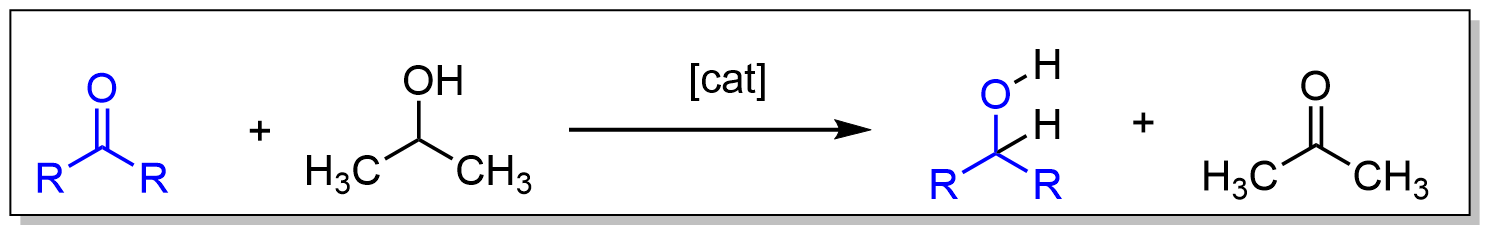
在化学中,氢转移氢化是一种化学反应,其中氢不是来自分子氢(H₂),而是来自其他来源。这种反应应用于实验室和工业有机合成,用于使有机化合物饱和,以及将酮还原为醇和亚胺还原为胺。氢转移氢化避免了传统氢化中使用高压分子氢的需求。 氢转移氢化通常在温和的温度和压力条件下进行,使用有机或有机金属催化剂,其中许多是手性的,从而实现高效的不对称合成。该方法使用氢供体化合物,例如甲酸、异丙醇或二氢蒽,将它们分别脱氢为二氧化碳(CO₂)、丙酮或蒽。[1] 在许多情况下,氢供体分子也充当反应的溶剂。氢转移氢化的一个大规模应用是使用“供氢溶剂”(如四氢萘)进行煤液化。[2][3]
有机金属催化剂
在有机合成领域,一类基于钌和铑配合物的高效氢转移催化剂家族已经被开发出来,这些催化剂通常含有二胺和膦配体。[4] 一个典型的催化剂前体来源于(cymene)钌二氯二聚体和对甲苯磺酰化二苯乙二胺。这些催化剂主要用于将酮和亚胺分别还原为醇和胺。氢供体(转移剂)通常是异丙醇,它在供氢后转化为丙酮。对于前手性底物,氢转移氢化可以以很高的对映选择性进行:

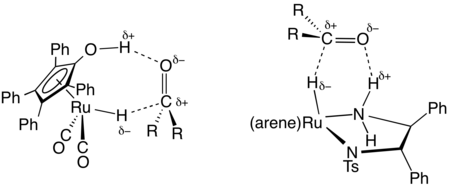
其中,RR'C*H−OH 是手性产物。一个典型的催化剂是(cymene)R,R-HNCHPhCHPhNTs,其中 Ts 表示对甲苯磺酰基(SO₂C₆H₄Me),R,R
表示两个手性碳中心的绝对构型。此项研究工作因其贡献而获得了 2001 年诺贝尔化学奖,由野依良治(Ryōji Noyori)主导完成。[5]
另一类氢转移试剂基于铝烷氧化物,例如 MPV 还原中的异丙醇铝。然而,与过渡金属基催化体系相比,这些试剂的活性相对较低。
使用基于 BINAP 的钌配合物首次展示了酮的催化不对称氢化。[6][7] 尽管 BINAP-Ru 二卤化物催化剂可以还原官能化酮,但对简单酮的氢化仍是一个难题。这一难题通过 RuCl₂(二膦)(二胺) 类型的催化前体得以解决。[8] 这些催化剂优先还原酮和醛,而对烯烃和许多其他取代基没有影响。
无金属催化氢转移反应
在催化氢化技术发展之前,已经开发了许多用于不饱和底物氢化的方法。这些方法中的许多现在仅具有历史和教学意义。一种重要的氢转移试剂是二亚胺(diimide),化学式为(NH)₂,也被称为偶氮烷(diazene)。该试剂在反应中被氧化为非常稳定的氮气 (N₂):
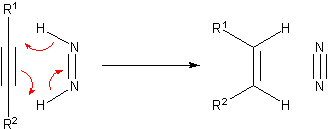
二亚胺可以通过肼(hydrazine)或某些其他有机前体生成。 两种可用作氢供体的烃是环己烯(cyclohexene)或环己二烯(cyclohexadiene)。在此反应中,会生成烷烃和苯。 当生成苯时,由于芳香稳定化能量的增加成为反应的驱动力。可以使用钯(Pd)作为催化剂,并在 100°C 的温度下进行反应。此外,还报道了一些更为特殊的氢转移反应,包括如下这种分子内的反应:
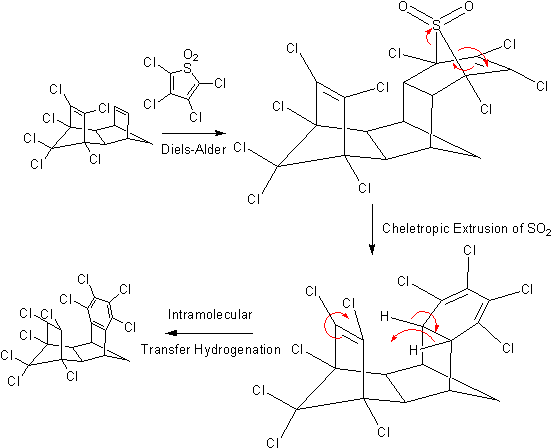
一些反应使用醇或胺作为质子供体,同时使用碱金属作为电子供体。仍然具有重要价值的是由金属钠介导的芳烃 (即芳香族碳氢化合物)的Birch还原反应。目前较不重要的是Bouveault–Blanc酯还原反应。镁和甲醇的组合可用于烯烃的还原,例如阿塞那平(asenapine)的合成:[11]
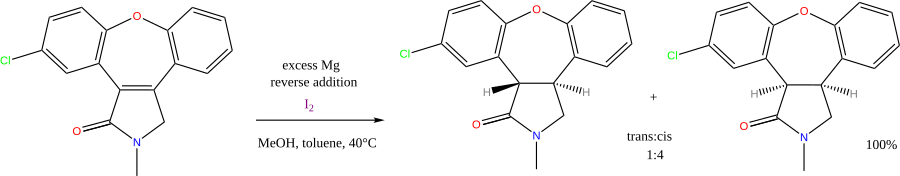
有机小分子催化的氢转移反应
由List团队在2004年提出了一种有机催化转移氢化反应系统,该系统使用Hantzsch酯作为氢化试剂,并以胺作为催化剂:[12]
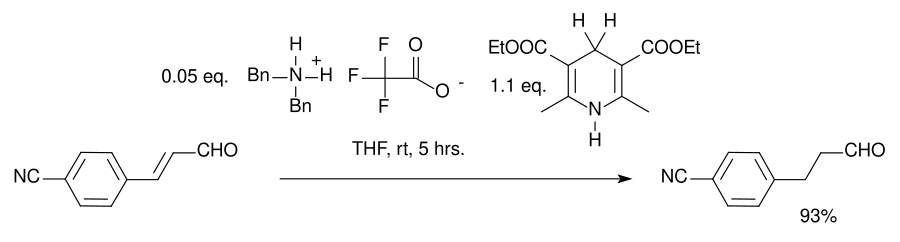
在这一反应中,底物是α,β-不饱和羰基化合物。质子供体被氧化为吡啶形式,与生物化学中相关的辅酶NADH类似。在该反应的催化循环中,胺和醛首先形成亚胺离子,随后发生质子转移,然后亚胺键水解以再生催化剂。通过采用手性咪唑烷酮MacMillan有机催化剂,可获得81% ee的对映选择性:
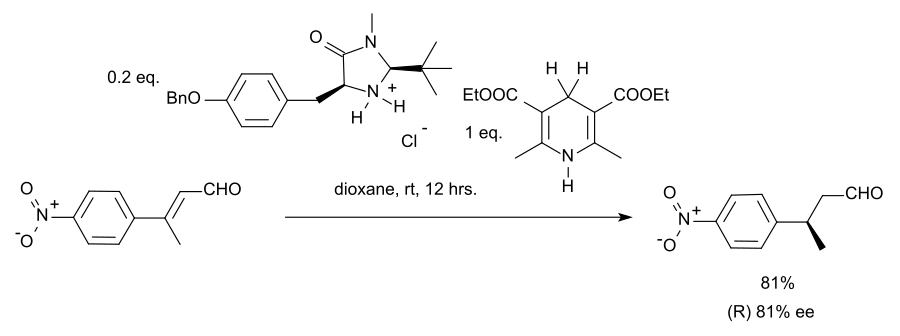
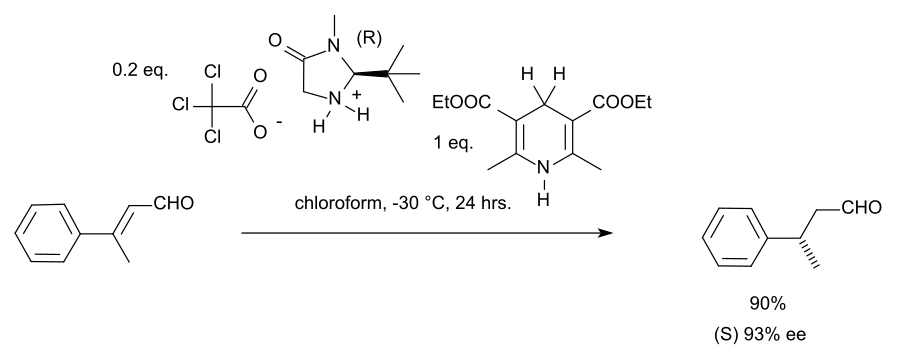
在立体收敛的情况下,该反应中的E-异构体和Z-异构体均产生(S)-对映体。
将此反应扩展到酮或酮类化合物(如烯酮)需要对催化剂进行微调(添加苄基并用呋喃取代叔丁基)以及对Hantzsch酯进行优化(添加更大的叔丁基):[14]
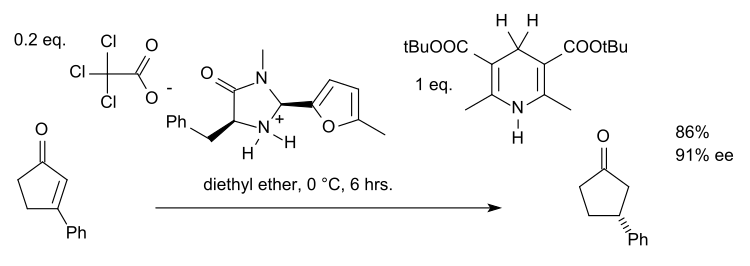
使用另一种完全不同的有机催化剂,氢化还可用于亚胺。一种串联反应由手性磷酸催化:[15]
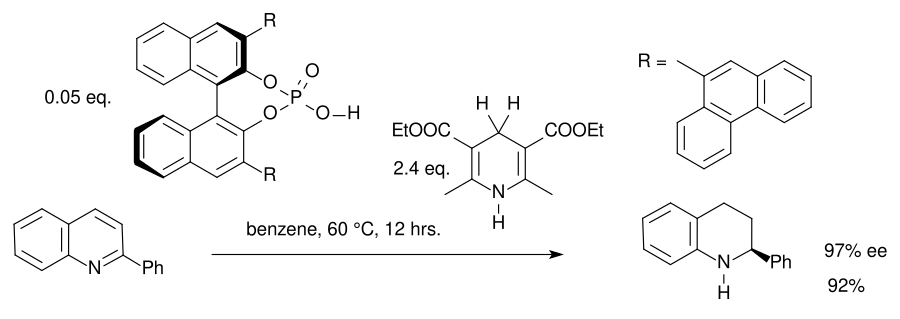
该反应通过手性亚胺离子进行。传统的金属催化剂在芳香族或杂芳香族底物的氢化反应中往往失败。
参考文献
1. Wang, Dong; Astruc, Didier (2015). "The Golden Age of Transfer Hydrogenation". Chem. Rev. 115 (13): 6621–6686. doi:10.1021/acs.chemrev.5b00203. ISSN 0009-2665.
2. Speight, J. G. "The Chemistry and Technology of Coal" Marcel Dekker; New York, 1983; p. 226 ff. ISBN 0-8247-1915-8.
3. Muñiz, Kilian (2005). "Bifunctional Metal-Ligand Catalysis: Hydrogenations and New Reactions within the Metal-(Di)amine Scaffold13". Angewandte Chemie International Edition. 44 (41): 6622–6627. doi:10.1002/anie.200501787. PMID 16187395.
4. T. Ikariya, K. Murata, R. Noyori "Bifunctional Transition Metal-Based Molecular Catalysts for Asymmetric Syntheses" Org. Biomol. Chem., 2006, 4, 393-406.
5. Shimizu, H., Nagasaki, I., Matsumura, K., Sayo, N., and Saito, T. "Developments in Asymmetric Hydrogenation from an Industrial Perspective" Acc. Chem. Res. 2007, vol. 40, pp. 1385-1393. doi:10.1021/ar700101x
6. Mashima, K.; Kusano, K.-h.; Sato, N.; Matsumura, Y.-i.; Nozaki, K.; Kumobayashi, H.; Sayo, N.; Hori, Y.; Ishizaki, T. (1994), "Cationic BINAP-Ru(II) Halide Complexes: Highly Efficient Catalysts for Stereoselective Asymmetric Hydrogenation of α- and β-Functionalized Ketones", The Journal of Organic Chemistry, 59 (11): 3064–3076, doi:10.1021/jo00090a026
7. Kitamura, M.; Ohkuma, T.; Inoue, S.; Sayo, N.; Kumobayashi, H.; Akutagawa, S.; Ohta, T.; Takaya, H.; Noyori, R. (1988), "Homogeneous Asymmetric Hydrogenation of Functionalized Ketones", Journal of the American Chemical Society, 110 (2): 629–631, doi:10.1021/ja00210a070
8. Noyori, R.; Ohkuma, T. (2001), "Asymmetric Catalysis by Architectural and Functional Molecular Engineering: Practical Chemo- and Stereoselective Hydrogenation of Ketones", Angewandte Chemie International Edition, 40 (1): 40–73, doi:10.1002/1521-3773(20010105)40:1<40::aid-anie40>3.0.co;2-5, PMID 11169691
9. Dub, Pavel A.; Gordon, John C. (2018). "The role of the metal-bound N–H functionality in Noyori-type molecular catalysts". Nature Reviews Chemistry. 2 (12): 396–408. doi:10.1038/s41570-018-0049-z. S2CID 106394152.
10. M. M. Midland (1989). "Asymmetric reductions with organoborane reagents". Chemical Reviews. 89 (7): 1553–1561. doi:10.1021/cr00097a010.
11. Linden, M. V. D.; Roeters, T.; Harting, R.; Stokkingreef, E.; Gelpke, A. S.; Kemperman, G. (2008). "Debottlenecking the Synthesis Route of Asenapine". Organic Process Research & Development. 12 (2): 196–201. doi:10.1021/op700240c.
12. Yang; Hechavarria Fonseca, M.; List, B. (2004). "A metal-free transfer hydrogenation: organocatalytic conjugate reduction of alpha,beta-unsaturated aldehydes". Angewandte Chemie International Edition in English. 43 (48): 6660–6662. doi:10.1002/anie.200461816. PMID 15540245.
13. Ouellet; Tuttle, J.; MacMillan, D. (2005). "Enantioselective organocatalytic hydride reduction". Journal of the American Chemical Society. 127 (1): 32–33. doi:10.1021/ja043834g. PMID 15631434.
14. Tuttle; Ouellet, S.; MacMillan, D. (2006). "Organocatalytic transfer hydrogenation of cyclic enones" (PDF). Journal of the American Chemical Society. 128 (39): 12662–12663. doi:10.1021/ja0653066. PMID 17002356. S2CID 12456921.
15. Rueping; Antonchick, A.; Theissmann, T. (2006). "A highly enantioselective Brønsted acid catalyzed cascade reaction: organocatalytic transfer hydrogenation of quinolines and their application in the synthesis of alkaloids". Angewandte Chemie International Edition in English. 45 (22): 3683–3686. doi:10.1002/anie.200600191. PMID 16639754.