aza-Wittig reaction
重要性
[开创性文献1;综述2-11;理论研究12-17]
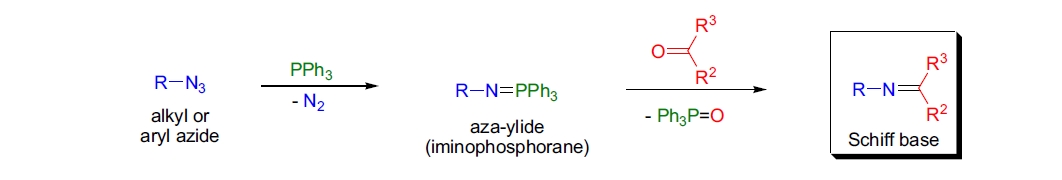
1919年,H. Staudinger和J. Meyer制备了PhN=PPh3,这是第一个aza-叶立德实例,也是第一个aza-Wittig试剂1。
叶立德的定义为“含有一个直接连接到带有较高正电荷的杂原子的负碳离子,其正电荷由取代基与杂原子的σ键形成”4。
aza-叶立德(亚胺膦)与各种羰基化合物的反应称为aza-Wittig反应,产物为席夫碱。与常规Wittig反应一样,副产物为三苯基膦氧。
过去十年中,由于其在含C=N双键化合物特别是含氮杂环合成中的实用性,aza-Wittig方法学引起了广泛关注。
分子内aza-Wittig反应是合成五元、六元、七元和八元杂环的有力工具。
机理18,15
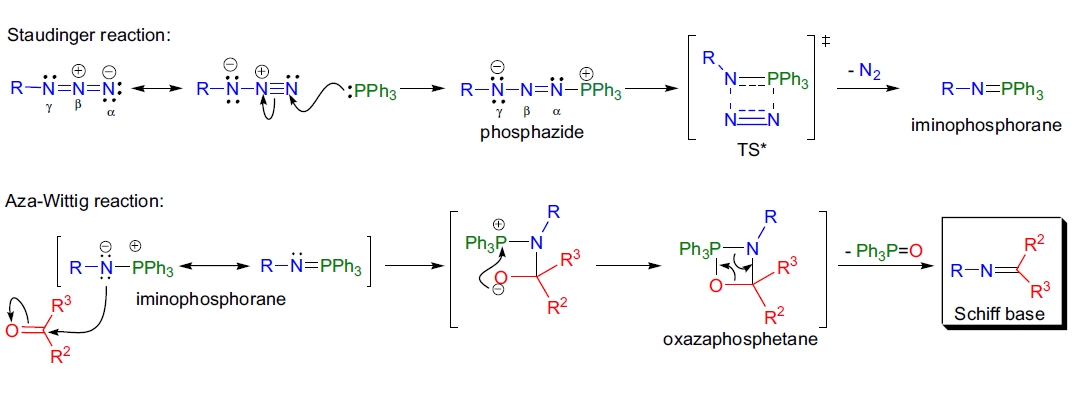
在第一步中,三苯基膦与烷基叠氮化物反应,失去氮气形成亚胺膦(Staudinger反应)。
在第二步中,亚胺膦的亲核氮进攻羰基,形成一个四元中间体(氧氮膦杂环丁烷),随后释放席夫碱产物和三苯基膦氧副产物。
合成应用
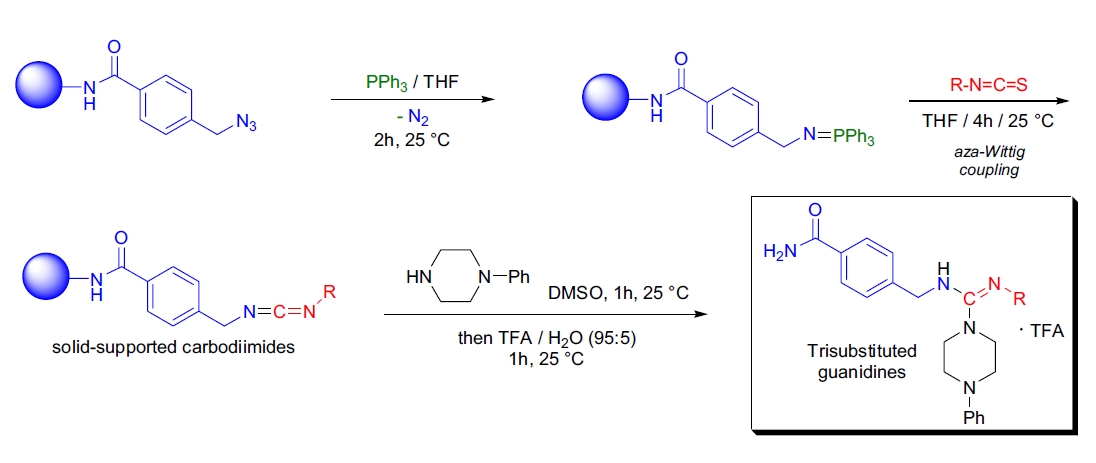
D.H. Drewery研究组利用aza-Wittig反应实现了三取代胍的固相合成。固相支撑的烷基亚胺膦与芳基或烷基异硫氰酸酯反应生成二亚胺,然后与伯胺或仲胺处理,得到三取代胍19。
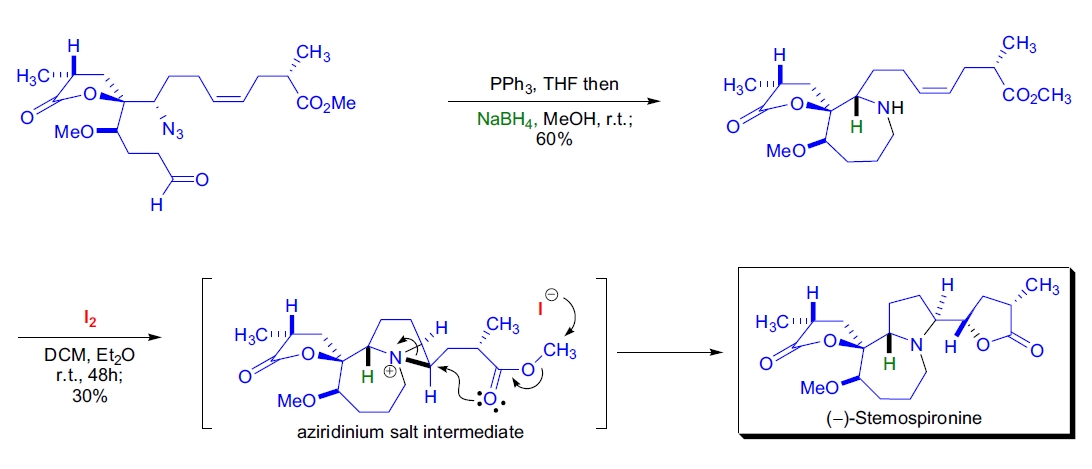
D.R. Williams等人完成了多环Stemona生物碱(–)-stemospironine的立体控制全合成20。
关键转化包括Staudinger反应生成aza-Wittig环闭合的过氢氮杂庚环体系。
Staudinger反应通过加入三苯基膦启动,生成aza-叶立德进行分子内缩合,得到七元亚胺。
随后原位还原得到氮杂环庚烷体系,最终通过碘诱导的双环化反应形成吡咯烷丁内酯的顺式选择性。
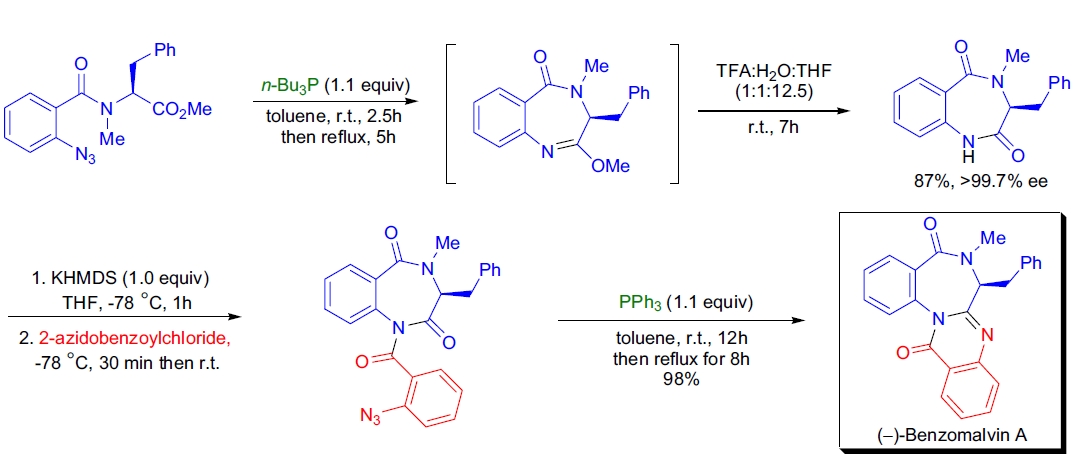
S. Eguchi实验室完成了(–)-benzomalvin A的首次全合成,该化合物具有4(3H)-喹唑啉酮和1,4-苯并二氮杂卓-5-酮结构单元21。
通过分子内aza-Wittig反应高效构建了六元和七元环骨架。前体由L-苯丙氨酸制备。
叠氮衍生物与三丁基膦反应生成相应的亚胺膦中间体,该中间体自发发生aza-Wittig环化反应,生成七元环。
最后,另一个分子内aza-Wittig环化反应构建了(–)-benzomalvin A的六元环。
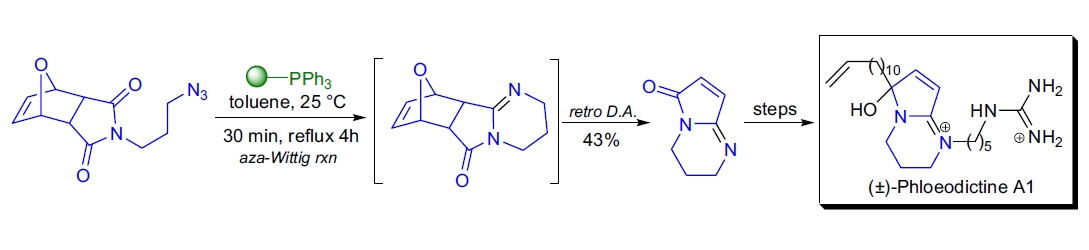
在B.B. Snider及其团队完成的抗肿瘤抗生素(±)-phloeodictine A1的全合成中,关键步骤是aza-Wittig反应,随后进行逆Diels-Alder反应,得到所需的双环亚胺22。
聚苯乙烯支撑的PPh3通过简单过滤方便地从副产物中分离出产物。