Eschenmoser-Tanabe 裂解
重要性
[开创性文献1,2;综述3,4;改进与优化5]
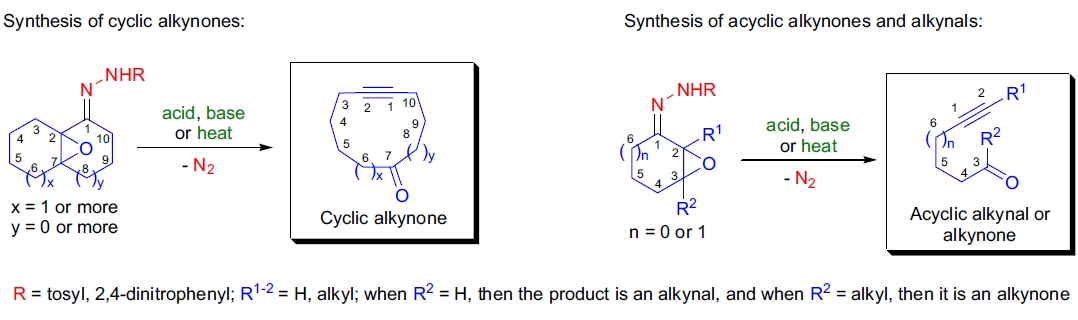
1967年,A. Eschenmoser 首次报道了 α,β-环氧酮的对甲苯磺酰腙发生裂解生成相应的炔酮(炔基酮)的反应1。不久后,M. Tanabe 和 J. Schreiber 分别独立发表了类似的裂解反应,用于生成中型环炔酮2-4。如今,通过环氧酮腙制备环炔酮、链式炔醛和炔酮的方法被称为 Eschenmoser-Tanabe 裂解。尽管该裂解反应可以发生在链状环氧酮腙上,但从合成的角度出发,需要以环状环氧酮为起始原料,以便获得目标的环炔酮或链式炔酮。环状环氧酮通常通过相应的 α,β-不饱和酮的环氧化反应制备13。
机理
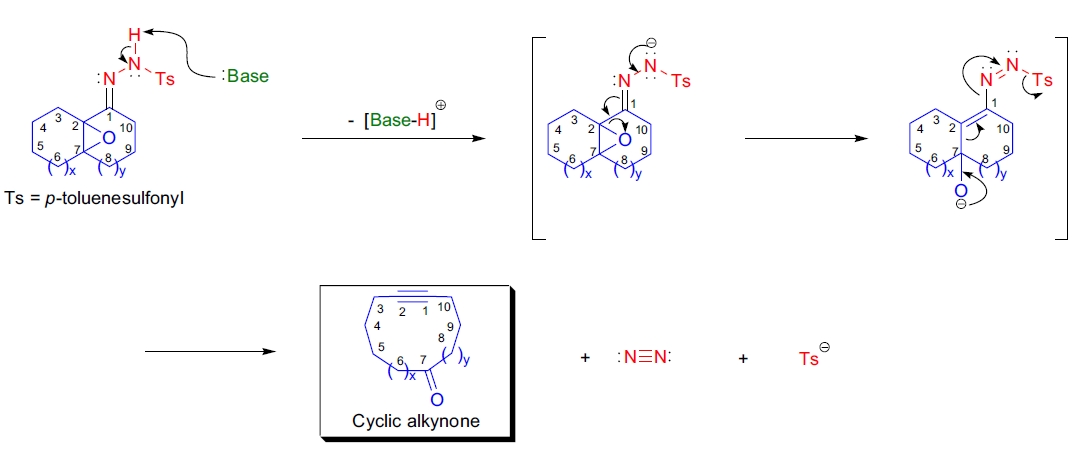
Eschenmoser-Tanabe 裂解基本上是七中心 Grob 型裂解,其中起始分子裂解为三个片段。对于环氧酮腙和氧二唑啉酮的裂解,机理是协同的;而对于环氧二氮杂环丙烷的热分解,则涉及一个自由氧杂环丙烷卡宾中间体18,19。环氧酮芳基腙的去质子化生成烷氧负离子,该负离子迅速发生裂解,生成炔烃、酮、氮气和一个离去基团(通常为芳基磺酸根)。
合成应用
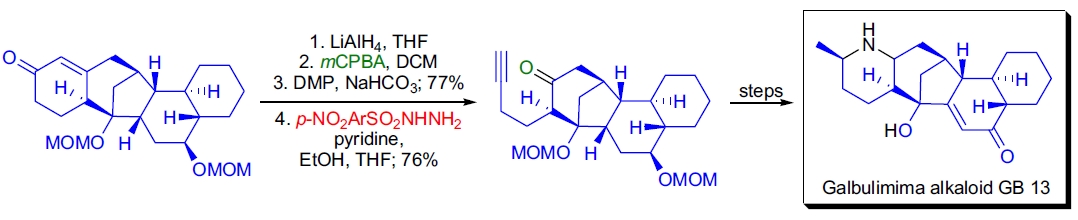
1. Galbulimima 生物碱 GB 13 的全合成: L.N. Mander 的研究团队在合成的后期将五环 α,β-不饱和酮转化为相应的四环炔酮,采用了 Eschenmoser-Tanabe 裂解法。直接对烯酮进行环氧化未能成功,因此通过还原-环氧化-氧化的序列获得了77%产率的目标环氧酮。环氧酮与对硝基苯磺酰肼反应,裂解得到炔酮20。
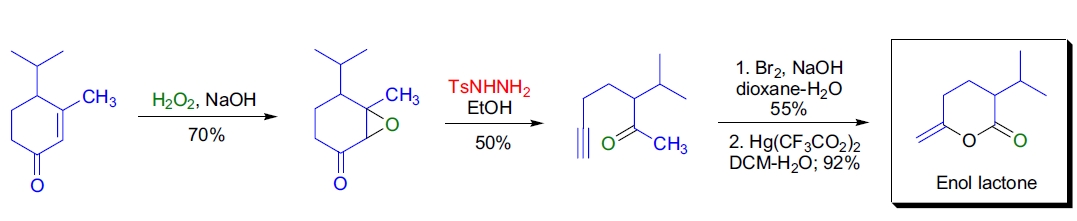
2. 弹性蛋白酶抑制剂的合成: J.A. Katzenellenbogen 等开发了一种高效合成烯醇内酯的方法。烯醇内酯的前体为 α-和 β-烷基取代的 5-己炔酸,这些化合物通过相应的烷基甲基酮的溴仿反应制备,而这些炔酮则通过 Eschenmoser-Tanabe 裂解法得到21。
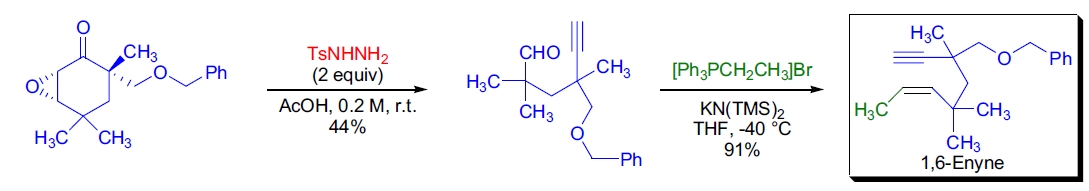
3. Botrydiane 抗生素的模型研究: B.M. Trost 等人制备了一种复杂的 1,6-炔烯前体,用于过渡金属催化的炔烯复分解反应。该 1,6-炔烯由重取代炔醛制备,而炔醛通过环氧酮的 Eschenmoser-Tanabe 裂解得到22。
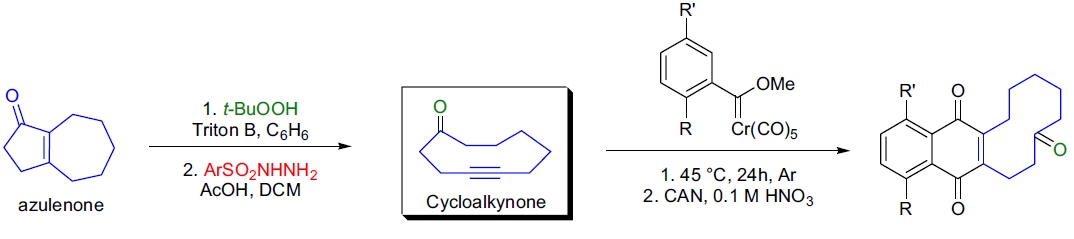
4. 含苯并[a]蒽核结构抗生素的合成: 在 S.J. Danishefsky 的实验室中,通过 Dötz 苯并环化反应研究了含苯并[a]蒽核心结构抗生素的合成。所需的环炔酮由 Azulenone 经 Eschenmoser-Tanabe 裂解法制备23。