Negishi交叉偶联反应
重要性
[开创性文献1-6;综述7-24;改进与优化25-32]
背景与历史
1972年,在发现镍催化的烯基和芳基卤化物与格氏试剂偶联反应(Kumada偶联反应 )后,人们认识到,为了提高这一过程对官能团的耐受性,需要使用比锂和镁更不电正的金属的有机试剂。 1976年,E. Negishi和其团队报道了第一例烯基铝试剂与烯基或芳基卤化物的立体专一性镍催化交叉偶联反应。1,2 Negishi进一步研究表明,在钯(0)催化剂存在下,使用有机锌试剂可以获得更好的反应速率、产率和立体选择性。3,4,7
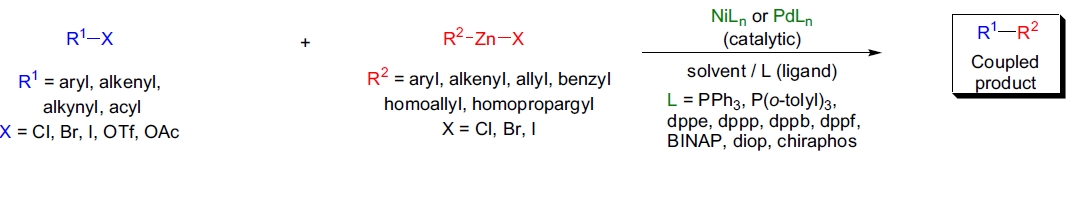
反应概述
Negishi交叉偶联反应具有以下特点:
- 镍和钯的膦配合物均可作为催化剂,钯催化剂通常具有更高的产率和功能团耐受性。
- 活性催化剂为不稳定的Ni(0)和Pd(0)配合物,可通过Ni(II)或Pd(II)配合物与还原剂(如DIBAL-H或n-BuLi)原位生成。
- 在没有过渡金属催化剂的情况下,有机锌试剂几乎不与烯基卤化物反应。
- 常用配体为PPh3,但也成功使用了其他手性和非手性膦配体。
- 有机锌试剂可以通过卤化物与锌金属直接反应或格氏试剂与锌卤化物的转金属化制备。
- 与Kumada偶联中使用的有机锂和格氏试剂相比,有机锌试剂具有更高的官能团耐受性。
- 该反应通常用于两个C(sp2)碳之间的偶联,但C(sp2)-C(sp)和C(sp2)-C(sp3)偶联也已被广泛研究。
该反应的一些局限性包括:
- 炔丙基锌试剂反应效果不佳,但同炔丙基锌试剂表现良好。
- 二级和三级烷基锌可能发生异构化,但一级烷基和苄基锌试剂的交叉偶联效果良好。
- 由于有机锌的高反应性,通常不会发生一氧化碳插入反应。
机理
[参考文献10]
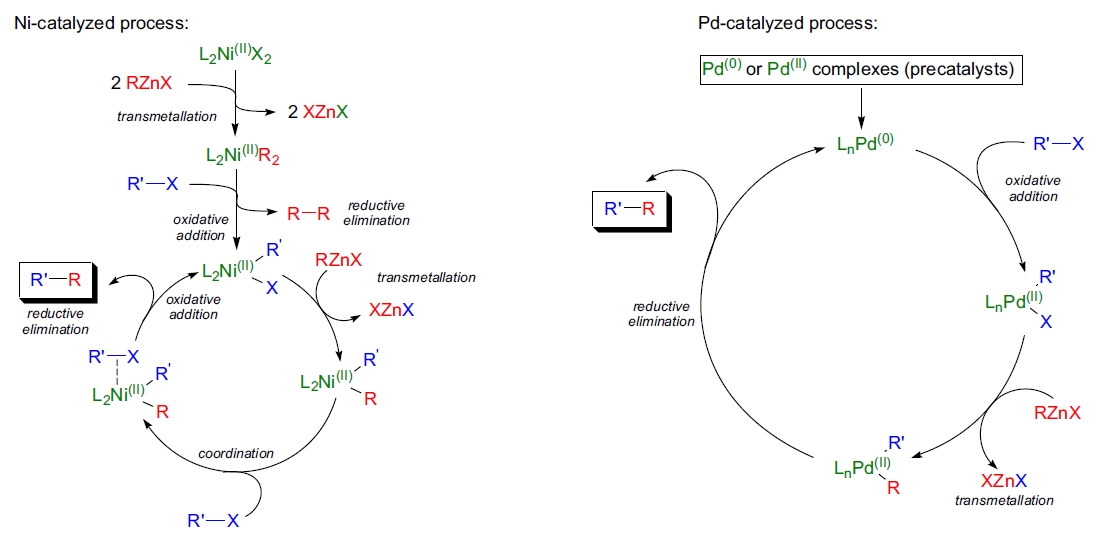
Negishi交叉偶联反应的机理包括以下步骤:
- 催化剂与卤化物发生氧化加成生成金属有机中间体。
- 随后进行转金属化过程,生成新的有机金属化合物。
- 通过还原消除步骤生成目标偶联产物,同时再生催化剂。
合成应用
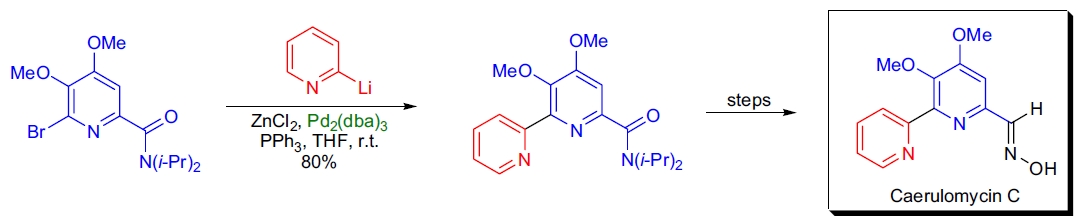
1. caerulomycin C的全合成: T. Sammakia 团队利用Negishi交叉偶联反应合成了bipyridyl结构,使用Pd2(dba)3/PPh3催化剂系统将6-溴吡啶与2-锌化吡啶偶联,获得高产率的目标产物。36
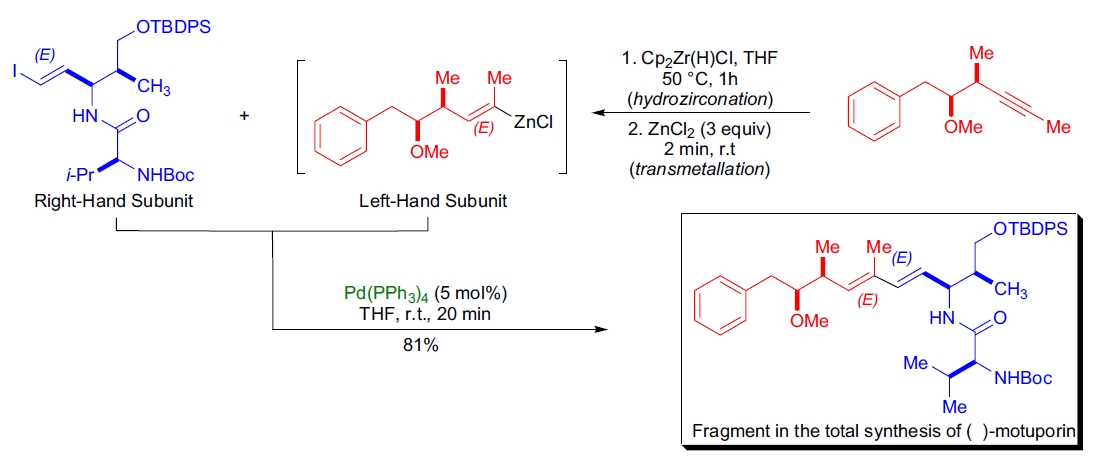
2. (–)-motuporin的全合成: J.S. Panek 等通过修饰的Negishi交叉偶联反应,将左手亚单元的有机锌化物与右手亚单元的(E)-烯基碘偶联,获得(E,E)-二烯产物,具有完全立体选择性。37
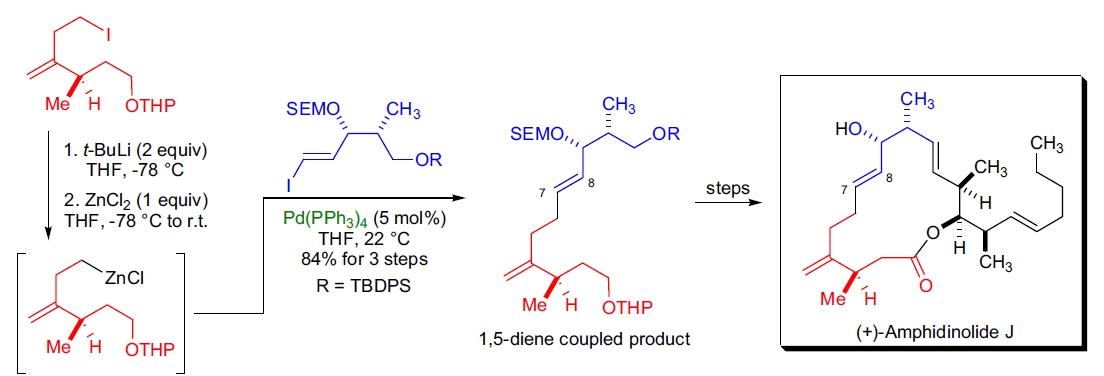
3. (+)-amphidinolide J的全合成: D.R. Williams 团队使用Negishi交叉偶联反应在高产率下合成了(E)-C7-C8双键。38