Horner-Wadsworth-Emmons 烯化反应
重要性
[开创性文献1-4;综述5-24;改进与优化25-39;理论研究40-46]
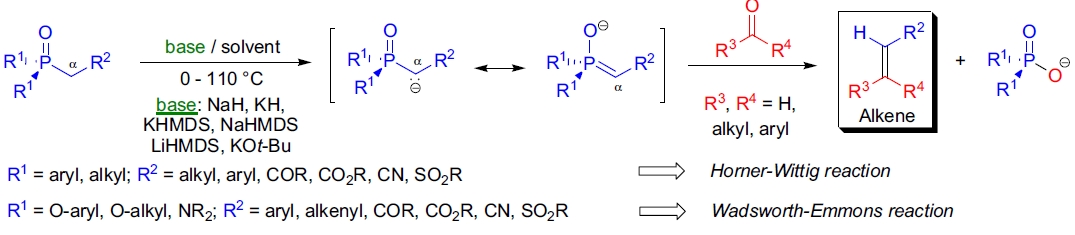
1958年,L. Horner 利用二苯基磷氧烷基化合物(R₁=Ph)的碳负离子制备醛和酮的烯烃衍生物1,2。这一对 Wittig 反应的改进被称为 Horner-Wittig 反应,但直到20世纪60年代初 W.S. Wadsworth 和 W.D. Emmons 研究了膦酸酯碳负离子(R₁=O-烷基)的合成应用后,该反应才广泛用于有机合成3。
HWE 烯化反应相比传统 Wittig 反应具有以下优势:
- 起始膦酸酯的制备更简单且更便宜(通常通过 Arbuzov 反应制备);
- 膦酸酯碳负离子比相应的磷亚甲基更具亲核性,因此可以在较温和条件下与几乎所有醛和酮反应;
- 在 Wittig 反应中不活泼的位阻较大的酮可以在 HWE 烯化反应中顺利反应;
- 膦酸酯阴离子的 α-碳可在烯化反应前进一步与各种亲电试剂(如烷基卤化物)反应,而磷亚甲基通常不能顺利烷基化;
- 副产物二烷基磷酸酯易溶于水,因此比难溶于水的三苯基氧化膦更易从烯烃产物中分离。
反应的主要特点包括:
- 对于二取代烯烃,在比 Wittig 反应更温和的条件下表现出高 (E)-选择性;
- 通过增加 R₁ 或 R₂ 的取代基尺寸(如 R=异丙基),可以最大化 (E)-选择性;
- 立体选择性强烈依赖于底物,但通过使用较小的取代基(如甲基)和强解离性碱(如 KOt-Bu),可以逆转生成以 (Z)-烯烃为主的产物。
主要改进包括:
- Still-Gennari 改进(R₁=OCH₂CF₃) 可专一生成 (Z)-烯烃27;
- 对于对碱敏感的底物,使用金属盐(如 LiCl 或 NaI)和弱胺类碱(如 DBU)可以避免外消旋化28,30,35;
- 对映选择性 HWE 烯化29,36,23;
- Corey-Kwiatkowski 改进使用磷酸酰胺类试剂制备 (Z)-烯烃,选择性极高25,26。
机理
[参考文献47,9,48,11]
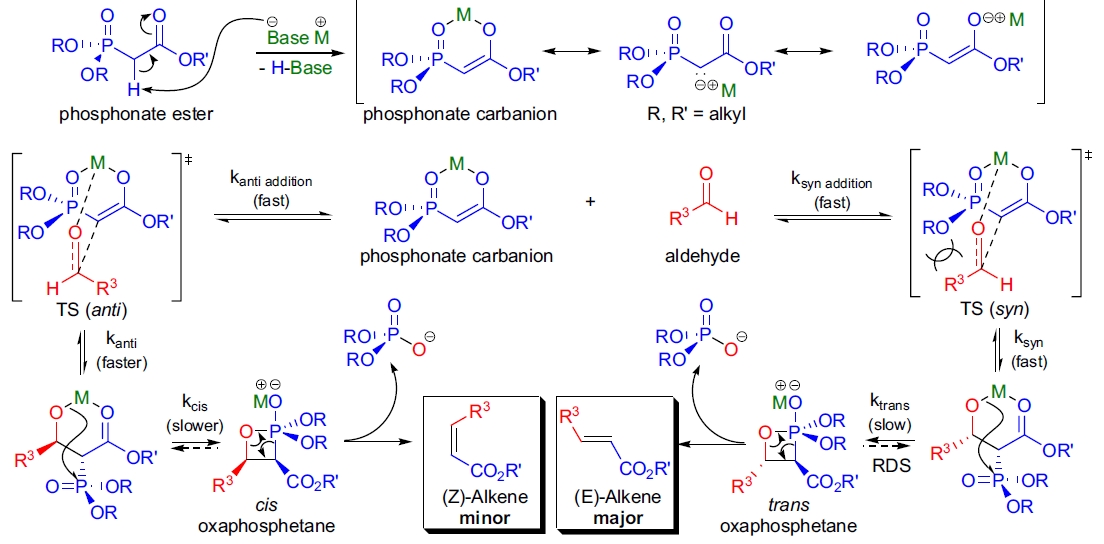
HWE 烯化反应的机理包括膦酸酯碳负离子的生成,其随后通过亲核加成与醛或酮反应形成 β-羟基膦酸酯中间体。接着,中间体发生消除反应,生成目标烯烃和二烷基磷酸酯副产物。
合成应用
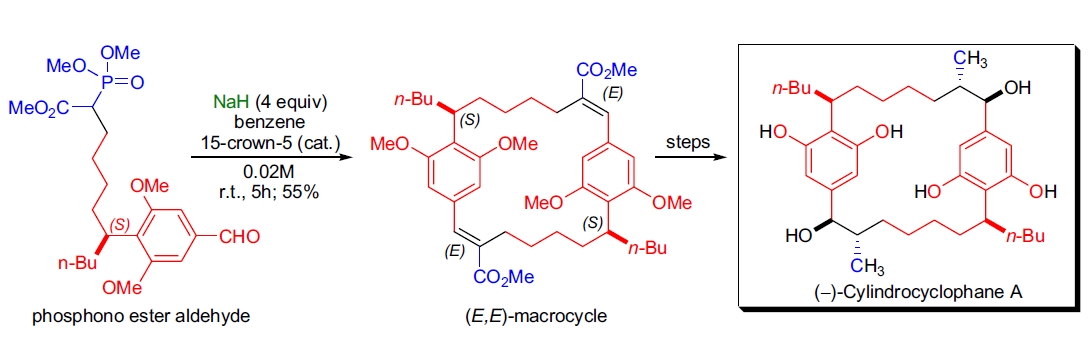
1. (–)-Cylindrocyclophane A 的全合成: T.R. Hoye 实验室通过 HWE 大环化尾-头二聚反应合成了 (–)-Cylindrocyclophane A 的 C₂-对称大环核心。将单体膦酸酯醛在苯溶剂中用 NaH 和催化量 15-冠-5 处理,生成的产物为 (E,E)-大环化合物,无 (Z,Z)-异构体生成,产率为 55%49。
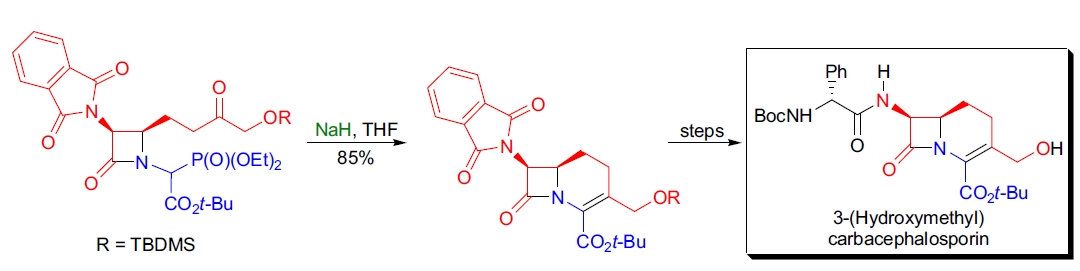
2. 碳青霉素抗生素的全合成: M.J. Miller 团队通过 Mitsunobu 环化形成 β-内酰胺环,并利用 HWE 环化构建六元不饱和环。该分子内烯化反应生成单一的二面体异构体,产率为 85%50。
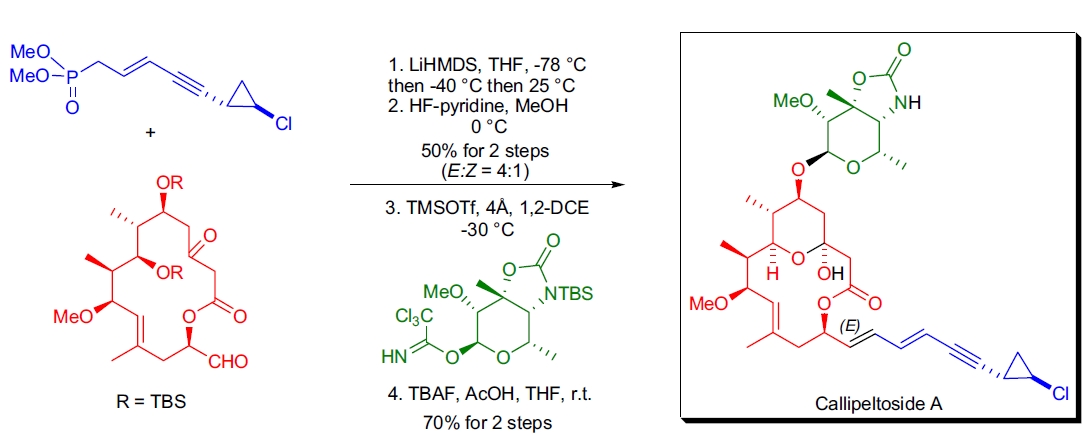
3. Callipeltoside A 的绝对构型研究: B.M. Trost 团队设计了高效的全合成策略,通过合成多个立体异构体来确定 Callipeltoside A 的绝对构型和相对构型。关键步骤包括钌催化的 Alder-ene 烯烃-炔烃偶联、钯催化的不对称烯丙基烷基化以及末端侧链的 HWE 烯化反应。烯化步骤生成的产物具有中等产率和 (E:Z = 4:1) 的中等立体选择性51。