Houben-Hoesch 反应
重要性
[开创性文献1-5;综述6-10;改进与优化11-17;理论研究18]
到20世纪初,Friedel-Crafts 酰化 和 Gattermann 甲酰化 分别被广泛用于制备芳香酮和醛。然而,对于高度活化的底物(如多酚类化合物),传统的 Friedel-Crafts 酰化条件通常会引入多个酰基,无法实现单一酰基化。
1915年,K. Hoesch 将 Gattermann 反应扩展至使用腈类而非氰化氢来制备芳香酮,并用较温和的氯化锌代替氯化铝1,2。十年后,J. Houben 对这一新型酮合成方法的适用范围和局限性进行了详细研究,并证明该方法主要适用于多酚或多烷氧基酚类化合物3。腈与多羟基或多烷氧基酚缩合生成相应的多羟基或多烷氧基酰氧基酮的反应被称为 Houben-Hoesch 反应。
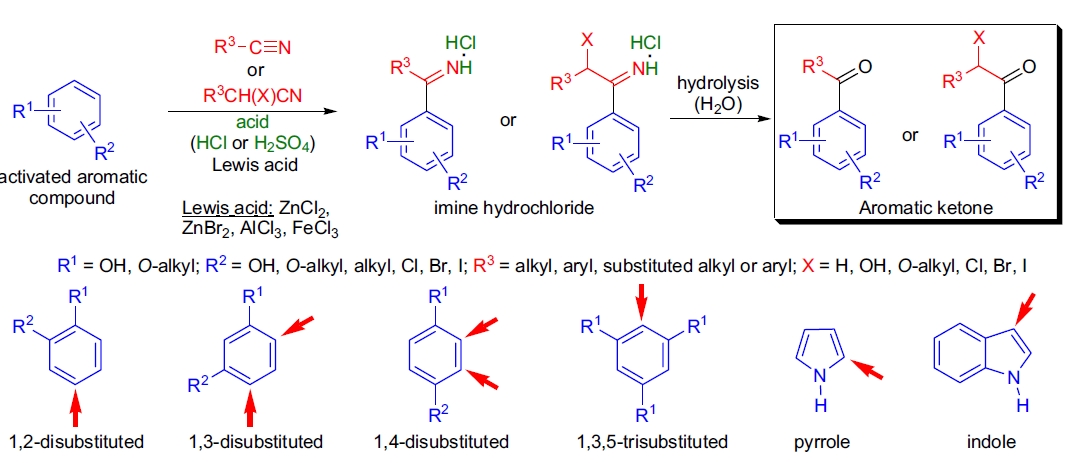
反应的主要特点包括:
- 仅高度活化的二取代芳香化合物可发生反应(至少一个取代基应为羟基或烷氧基);
- 芳香化合物可以是杂环化合物,因此吡咯、吲哚和呋喃也可作为底物;
- 腈的结构高度多样化:烷基、芳基及取代烷基(如 α-卤腈、α-羟腈及其醚和酯)均可兼容;
- 脂肪族腈通常比芳香族腈具有更高的产率;
- 芳香族腈的邻位不能有强吸电子基团(否则不发生反应),但这些基团位于间位则不影响反应性;
- 腈通常以其盐酸盐形式引入11;
- 氯化锌是最常用的路易斯酸,但对于非常电子丰富的底物(如三羟基苯),不需要使用路易斯酸;
- 反应的初始产物为亚胺盐酸盐,水解后生成最终产物芳香酮。
主要改进包括:
- 使用三氯乙腈,可使非活化芳香化合物也实现酰化;
- 用 BCl₃ 替代氯化锌,可使芳香胺实现高邻位选择性酰化13。
机理
[参考文献19,15,20,21]
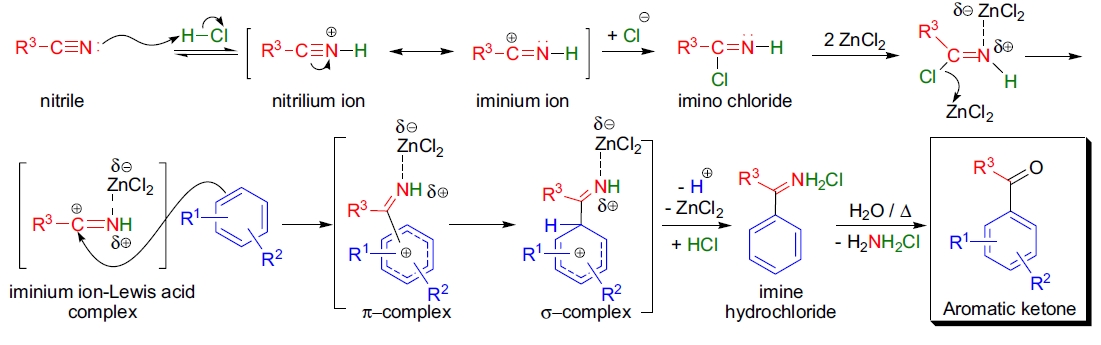
Houben-Hoesch 反应的机理尚未完全阐明,但与 Gattermann-Koch 甲酰化机理非常相似。第一步是生成腈离子氯化物,该中间体进一步转化为亚胺氯化物,从而生成反应活性种亚胺阳离子。
合成应用
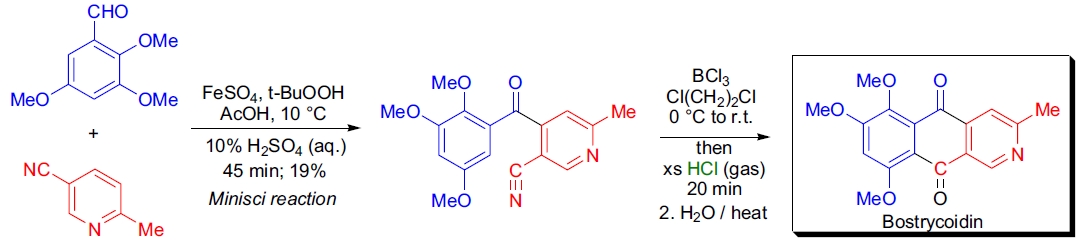
1. Bostrycoidin 的全合成: D.W. Cameron 实验室通过 Minisci 反应和分子内 Houben-Hoesch 反应完成了 azaanthraquinone 类天然产物 bostrycoidin 的全合成。值得注意的是,由于吡啶衍生物在酰化反应中的低反应性及取向特异性的缺乏,使用 Friedel-Crafts 酰化合成二羟基和三羟基 azaanthraquinone 非常有限22。
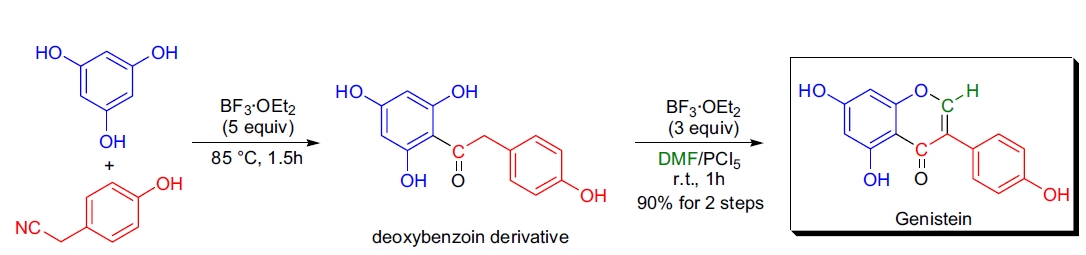
2. Genistein 的全合成: Genistein(4',5,7-三羟基黄酮)是一种重要的营养分子,存在于大豆种子中,具有广泛的药理作用。M.G. Nair 等通过两步合成法,用 Houben-Hoesch 反应使三羟基苯与对羟基乙腈酰化生成去氧苯偶姻,再用 DMF/PCl₅ 和 BF₃·OEt₂ 处理,最终生成 Genistein,产率为 90%23,24。
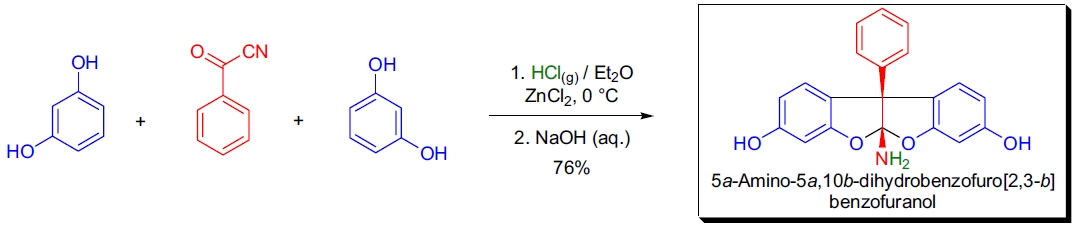
3. 异常产物的生成: 腈类化合物若在 α 或 β 位具有亲电基团或离去基团,常会生成“异常” Houben-Hoesch 产物。例如,α-羰基腈与酚反应可完全生成香豆素衍生物而非预期的1,2-二酮产物;α-卤腈与酚反应生成预期的 3-苯并呋喃酮及异常的 2-苯并呋喃酮。
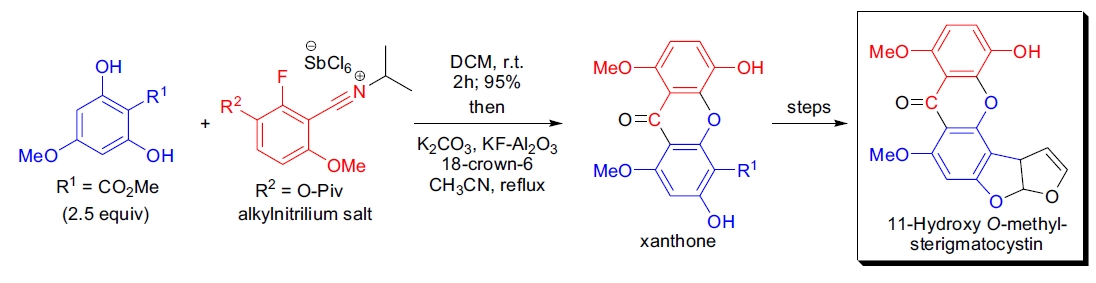
4. HOMST 的全合成: C.A. Townsend 实验室利用 Houben-Hoesch 反应的烷基腈离子变体合成了 11-羟基 O-甲基类固醇(HOMST)。烷基腈盐通过芳腈与 2-氯丙烯在 SbCl₅ 存在下制备,然后加入过量酚,碱性水解后生成黄酮类化合物,再经数步转化得到 HOMST17。